
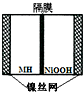
 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池 (MH-Ni碱性电池).下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池 (MH-Ni碱性电池).下列有关说法不正确的是( )| A、放电时正极反应为:NiOOH+H2O+e-=Ni(OH)2+OH- |
| B、放电时负极反应为:MH+OH--2e-=H2O+M+ |
| C、充电时氢氧根离子移向阳极,要参与电极反应 |
| D、充电时电池的正极连接直流电源的正极,得到电子发生还原反应 |


科目:高中化学 来源: 题型:
| A、3:2:1:4 |
| B、1:1:1:1 |
| C、2:1:2:2 |
| D、1:2:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定温度下,在固定体积的密闭容器中发生可逆反应A(s)+B(g)?C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态 | ||
| B、对于反应C(s)+CO2(g)?2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大 | ||
| C、室温下CH3COOH的Ka=1.7×10-5,NH3?H2O的Kb=1.7×10-5,CH3COOH溶液中的c (H+)与氨水中的c(OH-)相等 | ||
D、常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液后,溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用排饱和氯化钠溶液的方法收集氯气 |
| B、加催化剂,在一定条件下使N2和H2转化为NH3 |
| C、加压有利于SO2与O2反应生成SO3 |
| D、可用浓氨水和氢氧化钠固体来快速制取氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO42- |
| B、NO3- |
| C、SCN- |
| D、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液中加入过量的锌粉:Zn+2Fe3+═Zn2++2Fe2+ | ||||
| B、NH4Al(SO4)2中加入过量的NaOH溶液:Al3++4OH-═AlO2-+2H2O | ||||
| C、(CH3COO)2Ba中加入稀硫酸:Ba2++SO42-═BaSO4↓ | ||||
D、用惰性电极电解Cu(NO3)2溶液:2Cu2++2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.3mol/L |
| B、0.4mol/L |
| C、0.45mol/L |
| D、0.55mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com