
【题目】已知:CH3—CH=CH2+HBr―→CH3—CHBr—CH3(主要产物)。1 mol某烃A充分燃烧后可以得到8 mol CO2和 4 mol H2O。该烃A在不同条件下能发生如下图所示的一系列变化。
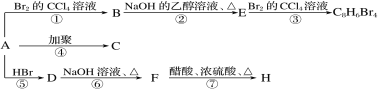
(1)A的化学式:________,A的结构简式:________。
(2)上述反应中,①是________反应(填反应类型,下同),⑦是________反应。
(3)写出C、D、E、H物质的结构简式:
C____________________,D_____________________,
E____________________,H_____________________。
(4)写出D―→F反应的化学方程式:_____________________。
【答案】C8H8 ![]() 加成 酯化(或取代)
加成 酯化(或取代) 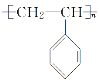
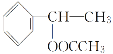
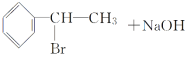
![]()
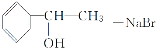
【解析】
1mol某烃A充分燃烧后可以得到8molCO2和4molH2O,故烃A的分子式为C8H8,不饱和度为(2×8+28)/2=5,可能含有苯环,由A发生加聚反应生成C,故A中含有不饱和键,故A为![]() ,C为
,C为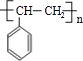 ,A与溴发生加成反应生成B,则B为
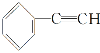
,A与溴发生加成反应生成B,则B为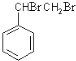 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成E,则E为
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成E,则E为![]() ,E与溴发生加成反应生成
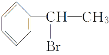
,E与溴发生加成反应生成![]() ,由信息烯烃与HBr的加成反应可知,不对称烯烃与HBr发生加成反应,H原子连接在含有H原子多的C原子上,故A与HBr放出加成反应生成D,则D为
,由信息烯烃与HBr的加成反应可知,不对称烯烃与HBr发生加成反应,H原子连接在含有H原子多的C原子上,故A与HBr放出加成反应生成D,则D为![]() ,D在氢氧化钠水溶液、加热条件下发生水解反应生成F,则F为
,D在氢氧化钠水溶液、加热条件下发生水解反应生成F,则F为![]() ,F与乙酸发生酯化反应生成H,故H为
,F与乙酸发生酯化反应生成H,故H为![]() 。
。
(1)由上述分析可知,A的分子式为C8H8,A的结构简式:![]() ;答案:C8H8;
;答案:C8H8;![]() ;
;
(2)上述反应中,反应①是A与溴发生加成反应生成B,反应⑦是F与乙酸发生酯化反应;答案:加成 ;酯化(或取代) ;
(3)由上述分析可知,C、D、E、H的结构简式分别是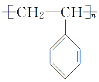 、
、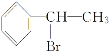 、
、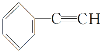 、
、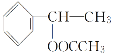 ;答案:
;答案:  ;
; ;
;  ;
; 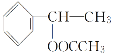 ;
;
(4)D→F是D在氢氧化钠水溶液、加热条件下发生水解反应生成F,反应方程式为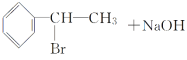
![]()
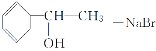 ;答案:
;答案:
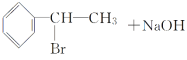
![]()
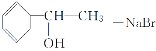 。
。


 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
【题目】某硫酸镁和硫酸铝的混合溶液中,c(Mg2+ )=2 mol·L-1,c(SO42-)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+分离,至少应加入1.6 mol·L-1氢氧化钠溶液的体积是
A.0.5 L B.1.625 LC.1.8 LD.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
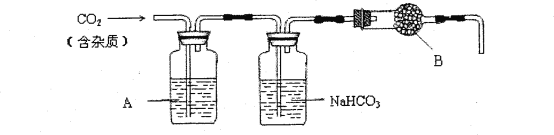
【题目】CaCO3广泛存在于自然界,是一种重要的化工原料。实验室用大理石(主要成分为CaCO3,另外有少量的含硫化合物)和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
完成下列填空:
(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6mol·L—1),应选用的仪器是____。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
上述装置中,A是___溶液,NaHCO3溶液可以吸收____。上述装置中,B物质是____。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果____(填“偏高”、“偏低”或“不受影响”)。
(2)SiO2与CO2组成相似,但固体的熔点相差甚大,其原因是_____。
(3)饱和的Na2CO3溶液中通入过量CO2的离子方程式为_____。0.1mol/L的NaHCO3溶液中,c(Na+)+c(H+)=_____,其中有关碳微粒的关系为:____ =0.1mol/L。浓度相等的Na2CO3和NaHCO3溶液等体积混合后,溶液中离子浓度由大到小的关系为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答一下回答以下关于第三周期元素及其化合物的问题。
(1)Na原子核外共有___种不同运动状态的电子,Al的原子结构示意图___。
(2)相同压强下,部分元素氟化物的熔点见表:

试解释上表中氟化物熔点差异的原因:___。
(3)SiF4分子的空间构型为____,SiF4中Si-F键间的键角是____。
(4)在P、S、Cl三种元素形成的氢化物中,热稳定性最大的是____(填氢化物的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚丙烯酸钠(![]() )具有超强吸水性,能吸收空气中的水分,可用于矿 山道路运输抑尘等。下列叙述不正确的是( )
)具有超强吸水性,能吸收空气中的水分,可用于矿 山道路运输抑尘等。下列叙述不正确的是( )
A. 聚丙烯酸钠属于纯净物 B. 聚丙烯酸钠可用于生产尿不湿
C. 聚丙烯酸钠的单体为CH2=CH—COONa D. 路面喷洒聚丙烯酸钠溶液能抑制扬尘,一定程度上能预防雾霾和 PM2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)![]() C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是( )
C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是( )
A.v(A)=0.2mol/(Ls)B.v(B)=0.6mol/(Ls)
C.v(C)=0.3mol/(Ls)D.v(D)=0.5mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3·5H2O),俗称大苏打,是无色透明晶体,易溶于水,易被氧化。是一种重要的化工产品,临床上用于氰化物的解毒剂,工业上也用于纸浆漂白的脱氯剂。某兴趣小组在实验室用如下装置(夹持仪器略去)模拟硫代硫酸钠生产过程。

(1)仪器a的名称为_________。
(2)装置A中发生反应的化学方程式为_____________________________。
(3)为提高产品纯度,应使烧瓶C中Na2S和Na2CO3恰好完全反应,则烧瓶C中Na2S和Na2CO3物质的量之比为____________。
(4)装置B中盛有饱和NaHSO3溶液,装置B的作用是_________、__________。
(5)装置D用于处理尾气,可选用的最合理装置(夹持仪器已略去)为____(填序号)。

(6)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
已知:Na2S2O3稀溶液与BaCl2溶液混合无沉淀生成。
限选试剂:稀HNO3、稀H2SO4、稀HCl、蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于A2(g)+3B2(g)![]() 2AB3(g)反应来说,以下化学反应速率的表示中,最快的是
2AB3(g)反应来说,以下化学反应速率的表示中,最快的是
A. v(A2)=0.008 mol·L-1·s-1B. v(A2)=0.3 mol·L-1·min-1
C. v(AB3)=0.01 mol·L-1·s-1D. v(B2)=0.012 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com