
常温下在20 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液40 mL,溶液的PH值逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示
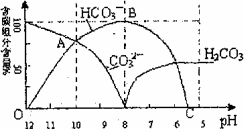
回答下列问题:
(1)在0.1mol/L Na2CO3溶液所有阳离子和阴离子的浓度有何关系?(用等式表示)___________.
(2)当加入盐酸使溶液PH值为10时,混合液中含碳元素的离子物质的量之比为________.
(3)随着盐酸的加入,请写出BC段的离子方程式______________.
(4)当混合液的PH=________时,开始放出CO2气体.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:上海市十三校2012届高三第二次联考化学试题 题型:021
|
常温下在20 mL 0.1 mol·L-1 Na2CO3溶液中逐渐滴加入0.1 mol/L HC1溶液40 mL,溶液的pH逐渐降低,下列说法正确的是(NA表示阿伏加德罗常数) | |
A. |
完全反应以后,溶液呈现中性 |
B. |
当盐酸加入20 mL时,溶液中NHCO3的物质的量为0.002NA |
C. |
20 mL 0.1 mol·L-1 Na2CO3溶液中c(Na+)+c(H+)=2c(CO |
D. |
20 mL 0.1 mol·L-1 Na2CO3溶液中c(H+)+2c(H2CO3)+c(HCO |
查看答案和解析>>
科目:高中化学 来源:天津市蓟县一中2011-2012学年高二上学期第三次月考化学试题 题型:022
| |||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省高考适应考试(一)理科综合化学试卷(解析版) 题型:选择题
常温下在20 mL 0.1 mol/L Na2CO3溶液中逐渐滴加入0.1 mol/L HCl溶液40 mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示,下列说法不正确的是
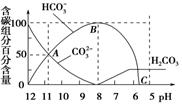
A.0.1 mol/L Na2CO3溶液中c(OH-)-c(H+)=2c(H2CO3)+c(HCO3-)
B.在A点c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
C.常温下CO2饱和溶液的pH约为5.6
D.0.05 mol/L NaHCO3溶液的pH=8
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com