
【题目】元素性质呈周期性变化的基本原因是
A.元素的原子量逐渐增大B.核外电子排布呈周期性变化
C.核电荷数逐渐增大D.元素化合价呈周期性变化
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( )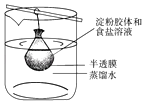
A.烧杯内液体加入硝酸银溶液后有白色沉淀产生
B.烧杯内液体加入碘水后呈蓝色
C.袋内液体加入硝酸银溶液后不会出现白色沉淀
D.袋内液体加入碘水后不变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在微生物作用下,电解有机废水(含CH3COOH),实现废水处理的同时,可获得清洁能源H2 . 其原理如图所示.下列有关说法正确的是( ) 
A.电极A为负极
B.电解中生成的CO2与H2物质的量之比为1:1
C.阳极反应为:CH3COOH一8e﹣+8OH﹣═2CO2↑+6H2O
D.电解前后,阴极室的pH几乎保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是短周期非金属元素,核电荷数依次增大.A元素原子核外有三种不同的能级且各个能级所填充的电子数相同,C是地壳中含量最多的元素.D、E是第四周期元素,其中E元素的核电荷数为29.D原子核外未成对电子数在同周期中最多.请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为 .
(2)B的氢化物易液化的原因是;
(3)已知A、C形成的化合物分子甲会造成温室效应,l mol甲中含有π键的数目为;
(4)基态D原子的外围电子排布式为 . DO2Cl2熔点:﹣96.5℃,沸点:117℃,则固态DO2Cl2属于晶体.
(5)E的氢化物的晶胞结构如图所示,其化学式是 . 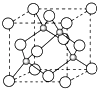
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在150℃时,(NH4)2CO3分解的方程式为:(NH4)2CO3 ![]() 2NH3↑+H2O↑+CO2↑,若完全分解,产生的气态混合物的密度是相同条件下氢气密度的( )
2NH3↑+H2O↑+CO2↑,若完全分解,产生的气态混合物的密度是相同条件下氢气密度的( )
A.96倍
B.48倍
C.12倍
D.10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能说明醋酸是弱电解质的是
A. 醋酸钠溶液呈碱性 B. 醋酸溶液中存在醋酸分子
C. 醋酸溶液导电性差 D. 0.1mol/L醋酸溶液的pH=2.9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丙苯( ![]() ),是一种重要的有机化工原料.根据题意完成下列填空:
),是一种重要的有机化工原料.根据题意完成下列填空:
(1)异丙苯的1H﹣NMR谱图中吸收峰的数目是组.
(2)工业上主要通过苯与丙烯通过分子筛固体酸催化剂工艺获得异丙苯,写出其方程式为 , 反应类型为反应.
(3)α﹣甲基苯乙烯( ![]() )是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法(用化学反应方程式表示).
)是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法(用化学反应方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组以废铁屑、稀硫酸、饱和(NH4)2SO4溶液为原料,经过一系列反应和操作后,合成了浅蓝绿色晶体X.为确定其组成,进行如下实验.
I.结晶水的测定:称取7.84g浅蓝绿晶体,加热至100℃失去结晶水,冷却至室温
后,称重,质量为5.68g.
Ⅱ.NH4+的测定:将上述5.68g固体置于如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入氮气,用40.00mL l molL﹣1的硫酸溶液吸收产生氨气.蒸氨结束后取下接收瓶,用2molL﹣1NaOH标准溶液滴定过剩的硫酸,到终点时消耗20.00mLNaOH溶液.
Ⅲ.铁元素的测定:将上述实验结束后三颈瓶中的溶液全部倒入锥形瓶中,向其中加入适量3%H2O2的溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后;测得其质量为1.6g. 回答下列问题:
(1)在实验I中,不可能用到的实验仪器是(填正确答案标号).
A.烧杯
B.铁架台(带铁圈)
C.坩埚
D.蒸发皿
E.酒精灯
F.干燥器
G.托盘天平
(2)在实验Ⅱ中,通入氮气的目的是 . 蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”,“处理”的操作方法是
(3)在实验Ⅱ中,用NaOH标准溶液滴定过剩的硫酸时,应使用式滴定管;可使用的指示剂为 .
(4)在实验中,检验沉淀是否洗净的方法是 .
(5)根据上述实验数据计算,该浅蓝绿晶体的化学式为 . 三颈瓶中发生反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com