
| 35L��6��10-3mol/L |
| 60L |
| 25L��0.012mol/L |
| 60L |
| Ksp |
| c(Cl-) |
| 1.8��10-10 |
| 1.5��10-3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� |
B�� |
C��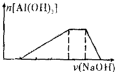 |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͬ�¶��£���Һ��ˮ�ĵ���̶ȣ���Һ�٣���Һ�� | ||
| B������������Һ�ٺ���Һ�ڣ�������Һ��c��Na+����c��CH3COO-����c��H+����c��OH-�� | ||
C����ˮϡ����Һ�٣���Һ��
| ||
D������Һ���м�������CH3COONa������
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧ�� | A-A | B-B | A-B |
| ����1mol��ѧ��ʱ�ų������� | 436kJ?mol-1 | 243kJ?mol-1 | 431kJ?mol-1 |
A��
| ||||
| B��A2��g��+B2��g���T2AB��g����H=-183kJ?mol-1 | ||||
C��
| ||||
| D��2AB��g���TA2��g��+B2��g������H=+183kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���ڢۢܢ� |
| C���٢ۢ� | D���٢ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2O2����������Ǽ��������� |
| B��Na2CO3���Ǽ��һ������ |
| C��NaOH��һԪ�ǿ�� |
| D��NaClO�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Q2��0.5Q1 |
| B��Q2��0.5Q1 |
| C��Q2=0.5Q1 |
| D��Q2=Q1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 3 |
| 2 |
A����NH4+ת��ΪNO3-���Ȼ�ѧ����ʽ�ɱ�ʾΪ��NH4+��aq��+2O2��g���TNO3-+2H+��aq��+H2O��l����H=-��b+
| ||
| B������������ת�������У���ˮ������������Ȼ������ | ||
| C�������£���HNO2��Һ��c��H+��=0.1 mol?L-1�������Һ��pH��1 | ||
| D������������ת����ȫ�������������������ӵĴ��ڣ���c��NH4+��+c��OH-���Tc��NO3-��+c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Բⶨijδ֪Ũ�ȵĴ�����Һ�д���ĵ��볣��Ka��Ӧ����ʵ���������Լ�������ֽ��Ϊ���к͵ζ�ʵ�顢pH��ֽ |
| B�������������£�CH3CO18OC2H5��ˮ�������CH3CO18OH��C2H5OH |
| C��C3H2Cl6�����ȴ��ﹲ��4�֣�����CH3-CH=CH-CH3��C3H6һ����Ϊͬϵ�� |
| D������0.1 mol/L��NaOH��Һ��0.5 mol/L��CuSO4��Һ���������Ƶ�������ͭ����Һ�����ڼ�����ѿ���ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com