
【题目】下列四种物质摩尔质量彼此接近。根据它们的结构判断,四种物质中,沸点最高、在水中溶解度最大的是( )
A.氯乙烷B.1-戊烯C.正戊烷D.1-丁醇
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】信息、材料、能源被称为新科技革命的“三大支柱”。下列有关资讯错误的是
A. 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B. 生活中常用的食品袋为聚乙烯产品
C. 随着人类文明逐渐发展,化石燃料将逐步退出历史舞台
D. 太阳能电池的主要材料是高纯度的二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为1L的干燥烧瓶中,用排空气法收集NH3气体,测得烧瓶中气体对氢气的相对密度为9.5,此气体中NH3的体积分数约为( )
A. 83% B. 75% C. 50% D. 25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是( )
A. 标准状况下,22.4LCCl4含有的分子数为 NA
B. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C. 通常状况下,NA个CO2分子占有的体积为22.4L
D. 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.烷烃分子中碳原子间以单键结合,碳原子剩余价键全部与氢原子结合
B.分子组成符合CnH2n+2的烃一定是烷烃
C.丙烷分子中三个碳原子在一条直线上
D.同分异构现象是有机物种类繁多的重要原因之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3、SiO2、Al2O3)为原料生产。实验室模拟工业法用铬铁矿制重铬酸钾(K2Cr2O7)的主要工艺如下:
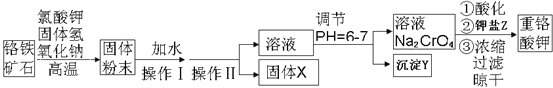
试回答下列问题:
(1)以上工艺流程所涉及元素中属于过渡元素的有_________。铁在周期表的位置是_________。
(2)煅烧前应将铬铁矿充分粉碎,其目的是___________________________。
如在实验室中将铬铁矿和NaOH固体混合物灼烧,从以下各实验仪器中选择必要有_________。
A.陶瓷坩埚 B.铁坩埚 C.三脚架 D.泥三角
(3)操作Ⅱ的名称是__________________。
(4)固体X的主要成分是__________________,沉淀Y的主要成分是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-氯乙基苯是一种重要的有机合成中间体,其一种制备反应原理为:

在T℃时,向2.0 L恒容密闭容器中充入0.40mol乙苯(g)和0.40mol Cl2(g)进行反应,反应过程中测定的部分数据见下表:
t/min | 0 | 1 | 2 | 5 | 10 |
n(HCl)/mol | 0 | 0.12 | 0.20 | 0.32 | 0.32 |
下列有关说法正确的是 ( )
A. 反应在0~2 min内的平均速率v(α-氯乙基苯)=0.10mol·L-1·min-1
B. 10 min后,若保持其他条件不变,升高温度,达到新平衡时测得c(α-氯乙基苯)=0.18mol·L-1,则反应的ΔH<0
C. 在T℃时,起始时若向容器中充入1.0 mol乙苯(g)、0.50 mol Cl2(g)和0.50 mol α-氯乙基苯(g)、0.50 mol HCl(g),则反应将向正反应方向进行
D. 在T℃时,起始时若向容器中充入2.0mol α-氯乙基苯(g)和2.2mol HCl(g),达到平衡时,α-氯乙基苯(g)的转化率小于20%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com