
 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.| FeBr3 |
| FeBr3 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、没有用浓硫酸作催化剂 |
| B、淀粉没有水解 |
| C、没有加入NaOH溶液中和溶液中的酸 |
| D、加入硫酸后不该加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氧 |
| B、1mol任何物质的质量都等于该物质的相对分子质量 |
| C、1molHCl气体的体积等于22.4L |
| D、氧气的摩尔质量为32g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
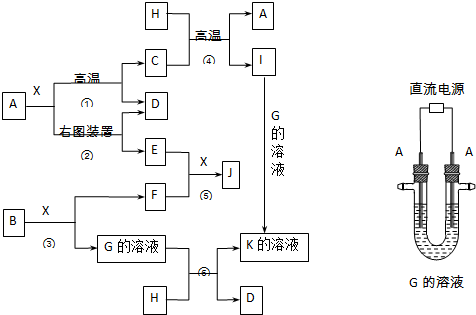
查看答案和解析>>
科目:高中化学 来源: 题型:
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两负电荷 | 0 |
| 丁 |
| 反应① |
| 丁 |
| 反应② |
查看答案和解析>>
科目:高中化学 来源: 题型:
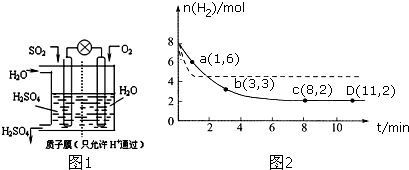
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com