
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两负电荷 | 0 |
| 丁 |
| 反应① |
| 丁 |
| 反应② |
| 14-2 |
| 2 |
| 14 |
| 2 |
 ,
,| m |
| M |
| 14g |
| 28g/mol |
| 14-2 |
| 2 |
| 14 |
| 2 |
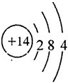 ;SiO2晶体中每个Si原子与4个O原子之间形成4个Si-O键,1molSiO2晶体中含有4NA个共价键,
;SiO2晶体中每个Si原子与4个O原子之间形成4个Si-O键,1molSiO2晶体中含有4NA个共价键, ;4NA;
;4NA; ,故答案为:
,故答案为: ;
;| m |
| M |
| 14g |
| 28g/mol |
| ||
| ||


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
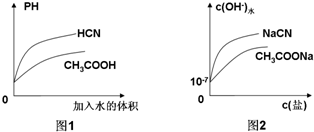
| A、常温下,等浓度的CH3COONa溶液和NaCN溶液的PH前者较小 |
| B、在NaCN溶液中:c (Na+)+c (H+)═c (OH-)+c (CN-) |
| C、相同温度下,相同PH的CH3COOH和HCN溶液分别加水稀释,溶液PH随溶液体积变化的曲线如图1所示 |
| D、常温下,CH3COONa溶液和NaCN溶液中由水电离出的c(OH-)与盐浓度的变化曲线如图2所示 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由N和H形成1 mol NH3所放出的能量 |
| B、把1 mol NH3中的共价键全部拆开所吸收的能量 |
| C、拆开NA个N-H键所吸收的能量 |
| D、形成1个 N-H键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
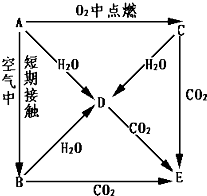 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A金属为单质.
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A金属为单质.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com