
9.75g锌与 mol的盐酸刚好完全反应,放出 mol H2,在溶液中有 mol Zn2+离子和 mol Cl-离子,把反应后的溶液蒸干,可以得到ZnCl2 mol。
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
在一定温度下,向密闭容器中充入1.0molN2和3.0molH2,反应达到平衡时测得NH3的物质的量为0.6mol。若在该容器中开始时充入2.0 molN2和6.0molH2,则平衡时NH3的物质的量 ( )
A、若为定容容器,n(NH3)=1.2mol B、若为定容容器,n(NH3)>1.2mol
C、若为定压容器,n(NH3) >1.2mol D、若为定压容器,n(NH3)<1.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L的恒容密闭容器中,充入0.2 molCO2和0.2 mol CH4,在一定条件下发生反应:CH4(g)+CO2(g) 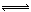 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是
A.上述反应的ΔH > 0
B.压强:P4 > P3 > P2 > P1
C.1100 ℃,P1时该反应平衡常数约为16.4
D.压强为p4时,在y点:V正 > V逆

查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的aL HCl气体溶于1000g水中,得到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是
A.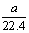 mo1·L-1 B.
mo1·L-1 B.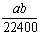 mol·L-1 C.
mol·L-1 C.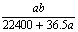 mol·L-1 D.
mol·L-1 D.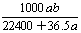 mol·L-1.
mol·L-1.
查看答案和解析>>
科目:高中化学 来源: 题型:
某盐的溶液中只含有Na+、Mg2+、Cl-、SO42- 四种离子,若有0.2mol Na+、0.4mol Mg2+、0.4mol Cl-,则SO42-的物质的量为
A. 0.1mol B. 0.3mol C. 0.5mol D. 0.15mol
查看答案和解析>>
科目:高中化学 来源: 题型:
用18 mol•L-1 浓硫酸配制100 mL 3.0 mol•L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是________,量取浓硫酸所用的量筒的规格是________(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)第③步实验的操作是________________________________。
(3)第⑤步实验的操作是________________________________。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中________________________________
B.容量瓶用蒸馏洗涤后残留有少量的水________________
C.所用过的烧杯、玻璃棒未洗涤________________
D.定容时俯视刻度线________________
查看答案和解析>>
科目:高中化学 来源: 题型:
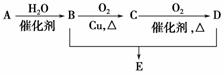
有机物A分子式为C2H4,可发生以下系列转化,已知B、D是生活中常见的两种有机物,下列说法不正确的是
A.75%的B溶液常用以医疗消毒
B.D、E都能与NaOH溶液反应
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.由B、D制备E常用浓H2SO4作脱水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列说法中,正确的是( )
A.常温常压下,3.0 g乙烷中含有的碳氢键数为0.7 NA
B.标准状况下,22.4 L C2H5OH中含有的氢原子数为6 NA
C.常温常压下,92 g的 NO2和N2O4 混合气体含有的原子数为 6 NA
D.标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3的沸点低于PH3 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com