
| ||
| ||
| ||
| 3a |
| 22.4 |
| △ |
| 0.75a |
| 22.4 |


科目:高中化学 来源: 题型:
| A、Y、Z、R的简单离子具有相同的电子层结构 |
| B、X、Z分别与Y均可形成A2B与A2B2型化合物,且A2B2均有较强的氧化性 |
| C、X2Y分子同存在氢键,故X2Y比X2W稳定 |
| D、由X、Y、Z形成的化合物能与X、Y、R形成的化合物发生复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8g氧-18气体的物质的量是0.1mol |
| B、0.1mol重氧气体的体积是2.24L |
| C、重氧气体的摩尔质量为36g |
| D、0.1mol重氧水所含中子数约是6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S8转化为S6、S4、S2属于物理变化 |
| B、不论哪种硫分子,完全燃烧时都生成SO2 |
| C、S8、S6、S4、S2均属于共价化合物 |
| D、把硫单质在空气中加热到750℃即得S2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物理性质 | 易溶于水,不溶于乙醇;熔点 48.2℃;在潮湿的空气中易潮解 |
| 化学性质 | 43℃以上的空气中易风化;遇酸易分解 (S2O32-+2H+=S↓+SO2↑+H2O ) |
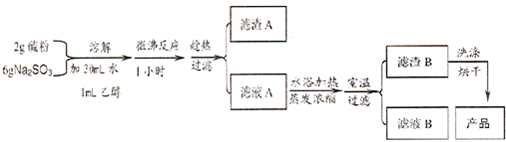
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
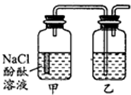 某课外活动小组,将剪下的一块镀锌铁放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )
某课外活动小组,将剪下的一块镀锌铁放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )| A、乙中导气管里形成一段水柱 |
| B、乙中导气管中产生气泡 |
| C、金属片剪口处溶液变红 |
| D、锌被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com