
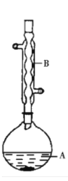
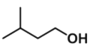
����Ŀ������������������۷���Ϣ�صijɷ�֮һ�������㽶����ζ��ʵ���ҿ��������������촼��Ũ������¼��ȷ�Ӧ�Ʊ�������������ʵ��װ��ʾ��ͼ���й��������£���ʵ����û�������Ϊ�ܼ���
 +
+
![]()
 +H2O
+H2O
���� | Ħ������(g/mol) | �ܶ�(g/mL) | �е�(��) | ˮ�е��ܽ��� |
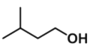
���촼 | 88 | 0.81 | 131 | �� |
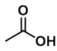
���� | 60 | 1.05 | 118 | ���� |
���������� | 130 | 0.80 | 142 | ���� |
������ | 84 | 0.78 | 81 | ���� |
ʵ�鲽�裺
����A�м��� 4.4 g �����촼��6.0 g �ı����ᡢ1.0 mL Ũ���ᡢ25 mL ������ͽ�����ӡ�������A�Ϸ���������B����֤ĥ�����ܣ���������װ�ù̶���
�ڴ������貢��������A��ֱ���ܼ���ʼ���������ִ��¶ȼ��ȣ�ά����ϵ���� 50 ���ӡ�
�۷�ӦҺ�������º����Һ©���У���25mLˮϴһ�Σ�����5%̼��������Һϴ�����ԡ�
���������ˮϴ���л���һ�Σ��ֳ��IJ������������ˮ����þ���壬����Ƭ�̡�
�ݹ��˳�ȥ����þ���壬�����������ռ�������֣������������� 3.51 g��
(1)����B ������Ϊ_____________��
(2)������У��ڡ��������貢��������A��ǰ����©��һ����Ҫ����������©���������ʵ��ʧ�ܲ�������ַ��ա�����©�IJ���Ϊ _______________________��
(4)�������ͨ�����������ղ�Ʒʱ��ʵ����Ӧ��_________�� �����ռ���Ʒ��ͨ�����㣬��ʵ��IJ�����_____________��
(5)����ʵ�ĺϳ�ʵ���У���������װ�� A ��װ�� B ֮������һ����ˮ��(��ͼ)�����������ԭ���ǣ��ܼ�������ͷ�Ӧ�����ɵ�ˮ�γɶ�Ԫ���������ʱ���߹�ͬ�������������������ˮ���С���ʱ��ˮ����Һ��Ҳ��ֲ㣬��������ˮ�ִ���_________��(ѡ���ϻ���)������������ԭ����֪����ˮ���ڴ�ʵ��������������________����ˮ������һ��Ҫ��;�ǹ۲�Ϳ��Ʒ�Ӧ���ȡ����豾ʵ����ʴﵽ 100%���ҷ�Ӧ���ɵ�ˮ��ȫ����������ȫ���������ˮ���пɷ���õ���ˮ�����Ϊ_____mL��(ˮ���ܶ�ȡ1.00 g/mL��������Ũ�����е�ˮ��)

���𰸡����������� ������������(B)��ͨ������ˮ ��ȥ��Ʒ�е�Ũ���ἰ�������� �����Ʒ 142 54% �� �����Ƴ���Ӧ�����ɵ�ˮ����ʹ��Ӧ������У���߲��� 0.9
��������
���촼���������ܽ��ڻ������У���Ũ���ᡢ������ӵĹ�ͬ�����£���������ͨ�����������ܵIJ����������ڷ�ˮ���������£����ܼ������ɵ�ˮ���Ϸֳ����Ӷ��ٽ����촼�������ķ�Ӧ���Ͻ��У�����ˮ����û��ˮ����ʱ��������Ӧ�Ѿ���ɣ���ʱֹͣʵ�飬��ȴ������Ʒ��ͨ��ˮϴ(ϴȥŨ����ʹ���)���ֳ��л�����ˮϴ(ϴȥ�ܽ��������)����ˮ����þ��ˮ�����˵Ȳ������õ���ˮ�л�������������롢���ռ�142 �����ҵ���֣��Ӷ���ò�Ʒ��
(1)����B �����������������õ���������������Ϊ���������ܡ���Ϊ�����������ܣ�
(2)�ڸ�������ƿ����ǰ����ͨ����ȴˮ������©�����ܻ��������ʵ��ʧ�ܲ�������ַ��գ�����©�IJ���Ϊ������������(B)��ͨ������ˮ����Ϊ��������������(B)��ͨ������ˮ��
(3)��Ӧ��������������Ũ���ᡢ������������ˮ������ˮϴ�ӣ����Բ������ˮϴ��Ŀ���dz�ȥ��Ʒ�е�Ũ���ἰ�������ˮϴ���л�������������ˮ�����Բ�����м�����ˮ����þ�����Ŀ���Ǹ����Ʒ����Ϊ����ȥ��Ʒ�е�Ũ���ἰ������������Ʒ��
(4)�������ͨ�����������ղ�Ʒ�����������������ķе�Ϊ142 ��������ʵ����Ӧ��142 �� �����ռ���Ʒ��n(���촼)=![]() =0.05mol��n(����)=
=0.05mol��n(����)=![]() =0.1mol�����Ա����������Ӧʹ�����촼���������������������ɷ�Ӧ����ʽ
=0.1mol�����Ա����������Ӧʹ�����촼���������������������ɷ�Ӧ����ʽ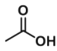 +
+
![]()
 +H2O���ɵó��������������������������ʵ���Ϊ0.05mol������Ϊ0.05mol��130g/mol=6.5g����ʵ��IJ�����
+H2O���ɵó��������������������������ʵ���Ϊ0.05mol������Ϊ0.05mol��130g/mol=6.5g����ʵ��IJ�����![]() =54%����Ϊ��142��54%��
=54%������142��54%��
(5)�ܼ���������ܶȱ�ˮС��������ˮ��λ���ϲ㣬���Է�ˮ���б�������ˮ�ִ����²㡣��ˮ����ʹ�л�����ˮ���룬���Է�ˮ���ڴ�ʵ�������������Dz����Ƴ���Ӧ�����ɵ�ˮ����ʹ��Ӧ������У���߲��ʡ����豾ʵ����ʴﵽ 100%���ҷ�Ӧ���ɵ�ˮ��ȫ����������ȫ���������ˮ���пɷ���õ���ˮ�����ʵ���n(H2O)= n(����������)=0.05mol�����Ϊ![]() =0.9 mL����Ϊ���£������Ƴ���Ӧ�����ɵ�ˮ����ʹ��Ӧ������У���߲��ʣ�0.9��
=0.9 mL����Ϊ���£������Ƴ���Ӧ�����ɵ�ˮ����ʹ��Ӧ������У���߲��ʣ�0.9��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʼ��仯�����ڻ�������������Ӧ�ù㷺��
(1)��ҵβ���е�SO2һֱ�ǻ�����Ⱦ����Ҫԭ��֮һ����ҵ�ϳ��������·�������β���еĺ�������
�ٷ���1��ȼú�м�����ʯ�ң���SO2ת��ΪCaSO3��������ΪCaSO4��
��֪��a��CaO(s)+CO2(g)=CaCO3(s) ��H= -178.3 kJ��mol-1��
b��2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)�� ��H= -2762.2 kJ��mol-1 ��
c��2CaSO3(s)+O2(g)=2CaSO4(s) ��H= -2314.8 kJ��mol-1 ��
д��CaO(s)��SO2(g)��Ӧ����CaSO3(s)���Ȼ�ѧ����ʽ��______��
�ڷ���2���ð�ˮ��SO2ת��ΪNH4HSO3��������Ϊ(NH4)2SO4��ʵ����NH4HSO3��Һ��![]() =1500������Һ��pHΪ_______��(��֪��H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)
=1500������Һ��pHΪ_______��(��֪��H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)
(2)ú�ƵõĻ���ԭ�����к����ʻ���(O=C=S)�������ʿ�ת��ΪH2S����ӦΪCOS(g)+H2(g)H2S(g)+CO(g)����H��0��
�ٺ��¡����������£��ܱ������з���������Ӧ��������ʵ����˵����Ӧ�ﵽƽ��״̬����__(����ĸ)��
a��COS��Ũ�ȱ��ֲ��� b����ѧƽ�ⳣ�����ٸı�
c�����������ܶȲ��ٸı� d���γ�2mol H-S����ͬʱ�γ�1 mol H-H��
��T1��ʱ���ں��ݵ��ܱ������У���������CO��H2S��ϼ��Ȳ��ﵽƽ�⣺H2S(g)+CO(g)COS(g)+H2(g)��K=0.25������¶��·�ӦCOS(g)+H2(g) H2S(g)+CO(g)��ƽ�ⳣ��K'=__��
��T1��ʱ�����ݻ�Ϊ10 L�ĺ����ܱ������г���1mol COS(g)��1mol H2(g)���ﵽƽ��ʱCOS��ת����Ϊ____��(������������С�����һλ)
(3)��������(H2S2O8)��һ��ǿ�������ᣬ��ṹʽΪ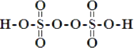 ����Ag+�������£�S2O82-����Mn2+��ˮ��Һ�з�����Ӧ����SO42-��MnO4-��1 mol S2O82-��������Mn2+�����ʵ���Ϊ__mol��
����Ag+�������£�S2O82-����Mn2+��ˮ��Һ�з�����Ӧ����SO42-��MnO4-��1 mol S2O82-��������Mn2+�����ʵ���Ϊ__mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼչʾ��ʵ������ȡ��������������ʵ��װ�á����й��ڸ÷�Ӧʵ����������������������ȷ����( )
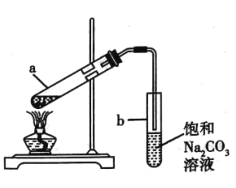
A.��a �Թ����ȼ����Ҵ���Ȼ������Ũ���ᣬ�ӱ����Թܣ����������ᡣ
B.�Թ�a ��ͨ��������������ᣬĿ����������Ҵ���ת����
C.�Թ�b �е������¶˹ܿڲ��ܽ���Һ�����£�Ŀ�����ڷ�ֹ����
D.��Ӧ���������۲쵽�Թ�b ����������ɫ�����������ù������ΪNaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��Ӧ 2NaCl(s) = 2Na(s)+Cl2(g)�� ��H��0, ��S��0
B. �����£���ϡCH3COONa��Һ��ˮϡ�ͺָ���ԭ�¶ȣ�pH�����Kw����
C. �ϳɰ������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����H2��ת����
D. ����ȼ�ϵ�ع���ʱ�������ı�״����11.2LH2����ת�Ƶ�����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ͻ���������й㷺Ӧ�ã�ij��ȤС��Ϊ���÷����������Ͻ����������ʵ�������Ʊ��ۺ���������������
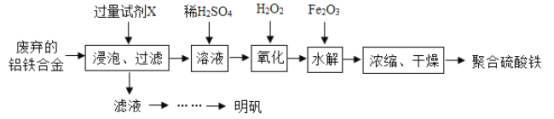
��1��������Ksp[Fe(OH)3]=4��l0-38�Ʊ�Fe(OH)3�Ĺ����У�pH=7ʱ��Һ��c(Fe3+) =________��
��2���ۺ���������һ���ެ��ѡ���ѧ�����ȶ�������ˮ���ܵ������������������Ҵ����仯ѧʽ�ɱ�ʾΪ[Fe2(OH)x(SO4)y]n��
��д�������е���������ʱ���������ӷ���ʽ_______��Ũ��ʱ�����м���һ�������Ҵ��������Ҵ���Ŀ����_________��
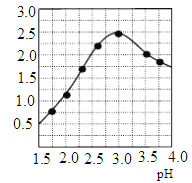
�ڼ����Լ�Y��Ŀ���ǵ���pH�������Լ�YΪ_______����ҺpH��[Fe2(OH) x (SO4)y]n��x��ֵ�нϴ�Ӱ�죨��ͼ��ʾ�����Է���pH��С��pH��3�����¾ۺ���������x��ֵ��С��ԭ��____________��
��3��������һ�ֳ������������Ρ�
��Ϊ�������ԭ�ϣ��Լ�XӦΪ_______��
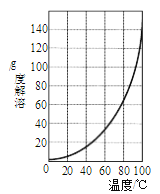
������ͼ��ʾ�������ܽ�����ߣ�������������ҺI�Ʊ����������ʵ�鲽��(��ѡ�õ��Լ��������������Ͻ�ϡ���ᡢNaOH��Һ�;ƾ�)������ҺI�м��������ĺ�������м�����������ݲ��������ˣ�_____������Һ_______�����ˡ����þƾ�ϴ�ӡ�������յõ��������塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ݻ�Ϊ2 L�ĺ����ܱ������м���0.2 mol CO��0.4 mol H2���������·�Ӧ��CO(g)��2H2(g)![]() CH3OH(g) ʵ����300���500���£��״������ʵ�����ʱ��ı仯���±���ʾ������˵����ȷ����
CH3OH(g) ʵ����300���500���£��״������ʵ�����ʱ��ı仯���±���ʾ������˵����ȷ����
10min | 20min | 30min | 40min | 50min | 60min | |
300�� | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
500�� | 0.120 | 0.150 | 0.156 | 0.160 | 0.160 | 0.160 |
A. �÷�Ӧ���ʱ䦤H > 0�������¶�K����
B. 300��ʱ��0��20 min H2��ƽ����Ӧ���� v ��H2��= 0.003mol/(L��min)
C. ��ȡ��ѹ������H2Ũ�ȡ���������Ĵ�ʩ�������CO��ת����
D. 500���£���������г�ʼ����0.1 mol CO��0.3 mol H2�������������ݿɼ��㷴Ӧ��ƽ���״���Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��Ϊ̽��AgCl�������ܽ��ת������ʵ�鷽������¼���£�
��������� | ���� |
�������������Ũ�ȵ�AgNO3��Һ��NaCl��Һ��ϣ����ˣ�����ҺX�Ͱ�ɫ����Y | |
��������ҺX �еμӼ��α���KI��Һ | ���ɻ�ɫ����M |
����ȡ������ɫ����Y���μӼ��α���Na2S��Һ | ����Y ת��Ϊ��ɫ����Z |
����ȡ������ɫ����Y���μӼ���Ũ��ˮ | ����Y���ܽ� |
(1)�ɲ�����������Ʋ⣬��Һ X �г��˺���Na+��NO3-�������е�������_____��
(2)д������������ɺ�ɫ���� Z �����ӷ���ʽΪ_________________����ɫ����Y ת��Ϊ��ɫ���� Z ����Ҫԭ����___________��
(3)��֪��Ag+ + 2NH3�� H2OAg(NH3)2++2H2O����ƽ���ƶ�ԭ�����Ͳ�����м���Ũ��ˮ�������ܽ��ԭ��__________________��
(4)Ϊ�˽�һ��̽���������ܻ���������ܽ�Ķ����ԣ���ͬѧ���������¶Ա�ʵ�� V��
��ȡ������ɫ���� Z �ͻ�ɫ���� M����������֧�Թ���
��Ȼ��ֱ�μ�ͬ���ͬŨ�ȵ�ϡ���ᣬ�۲쵽��ɫ���� M ���ܽ⣬��ɫ���� Z �ܽ⣬��������ɫ����������ۺ�ʵ�����ʵ�� V ����Ϣ������Ԥ����ȷ����__________
A����ɫ���� Z �Ȼ�ɫ���� M ��������ˮ
B����ɫ���� Z �ܽ���ϡ��������Ϊ������������ԭ��Ӧ
C���ɲ���������Ʋ⣺ʵ���ҿ��ð�ˮϴ��������Ӧ����Թ�
D���ڲ����֮�����μ�Ũ��������� AgCl ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ϩ�ĽṹΪ![]() ���йظ����ʵ�����˵����ȷ����
���йظ����ʵ�����˵����ȷ����
A. ��������ʹ��ˮ�������{�������Һ��ɫ����ɫԭ����ȫ��ͬ
B. ����ϩ���ӵ�����ԭ�Ӳ�������ͬһƽ����
C. �����ʱ����ϵ�һ��ȡ������3��
D. ��ȥ�ұ��л��еı���ϩ������ͨ�����������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��500 mL KNO3��Cu(NO3)2�Ļ����Һ��c(NO3-)��6.0 mol��L��1����ʯī���缫������Һ����ͨ��һ��ʱ����������ռ���22.4 L����(��״��)���ٶ�������Һ�����Ϊ500 mL������˵����ȷ����( )
A. ԭ�����Һ��c(K��)Ϊ2 mol��L��1
B. �����������й�ת��6 mol����
C. ���õ���Cu�����ʵ���Ϊ0.5 mol
D. ������Һ��c(H��)Ϊ2 mol��L��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com