
【题目】一种以2mol/L Na2SO4水溶液为电解质的钠离子电池的总反应如下:NaTi2(PO4)3 +Zn+ Na2SO4![]() Na3Ti2(PO4)3 +ZnSO4。其中P的化合价为+5,下列有关说法正确的是( )
Na3Ti2(PO4)3 +ZnSO4。其中P的化合价为+5,下列有关说法正确的是( )
A.放电时,NaTi2(PO4)3发生氧化反应
B.放电时,钠离子向负极移动
C.充电时,阳极反应式为:Zn-2e- =Zn2+
D.充电时,每移动0.2mol电子,消耗0.1mol Na3Ti2(PO4)3
【答案】D
【解析】
试题分析:A.放电时,化合价降低的Ti元素所在的反应物NaTi2(PO4)3发生还原反应,Ti元素的化合价由+4价变为Na3Ti2(PO4)3中的+3价,错误;B.原电池中,电解质里的阳离子移向正极,阴离子移向负极,所以钠离子移向正极,错误;C.充电时,阳极上发生失电子的氧化反应:Ti2(PO4)3 -2e-=Ti2(PO4)33 -,错误;D.根据电池反应:NaTi2(PO4)3 +Zn+ Na2SO4![]() Na3Ti2(PO4)3 +ZnSO4可知,若转移电子是2mol,即每移动2mol电子,消耗1mol Na3Ti2(PO4)3,所以每移动0.2mol电子,消耗0.1mol Na3Ti2(PO4)3,正确。
Na3Ti2(PO4)3 +ZnSO4可知,若转移电子是2mol,即每移动2mol电子,消耗1mol Na3Ti2(PO4)3,所以每移动0.2mol电子,消耗0.1mol Na3Ti2(PO4)3,正确。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效,苹果醋是一种常见的有机酸,其结构简式为

(1)苹果醋中含有的官能团的名称是________________。
(2)苹果醋的分子式为________。
(3)1 mol苹果醋与足量Na反应,能生成标准状况下的H 2 ________L。
(4)苹果醋可能发生的反应是________。
A.与NaOH溶液反应
B.与石蕊试液作用
C.与乙酸在一定条件下发生酯化反应
D.与乙醇在一定条件下发生酯化反应
(5)两分子苹果醋发生酯化反应成C8H10O9的链状酯有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共价键、离子键和范德瓦尔斯力都是微粒之间的不同作用力,下列含有上述两种结合力的是( )
①Na2O2 ②SiO2 ③石墨 ④金刚石 ⑤NaCl ⑥白磷.
A.①②④ B.①③⑥ C.②④⑥ D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,固定体积的密闭容器内,反应2HI(g)![]() H2 (g)+ I2 (g)达到平衡状态的标志是:( )
H2 (g)+ I2 (g)达到平衡状态的标志是:( )
①I2的体积分数不再变化;
②生成1 mol H2同时消耗1 molI2;
③容器内压强不再变化;
④生成2 mol HI同时消耗1molH2;
⑤气体的密度不再变化;⑥混合气体的平均分子质量不再变化
A.①②③④⑤⑥ B.①②③⑤⑥ C.①②⑤⑥ D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子核中的质子数或中子数为某些特定数值时,原子核就异常稳定,科学家将这些数值称为“幻数”,科学家在人造硅同位素1442Si中发现新的物理学“幻数”,下列有关1442Si的说法正确的是
A. 原子序数是42 B. 质量数是14 C. 中子数是42 D. 电子数是14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题满分18分)钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:

已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解.
请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有 ,操作2是 、过滤,副产品主要成分的化学式为 。
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理 。
(3)已知钛的还原性介于铝和锌之间,估计钛能耐腐蚀的原因之一是,如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式为 。
(5)为测定溶液中TiOSO4的含量,首先取待测钛液10mL用水稀释至100mL,加过量铝粉,充分振荡,使其完全反应:3TiO2++Al+6H+═3Ti3++AlO3++3H2O,过过滤后,取出滤液20.00mL,向其中滴加2~3滴KSCN溶液作指示剂,用 (填一种玻璃仪器的名称)滴加0.1000molL﹣1FeCl3溶液,发生Ti3++Fe3+═Ti4++Fe2+,当溶液出现红色达到滴定终点,用去了30.00mLFeCl3溶液,待测钛液中TiOSO4的物质的量浓度是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若平衡体系A+B![]() C+D,增大压强时反应速率变化如图所示。则下列关于各物质状态的说法正确的是( )
C+D,增大压强时反应速率变化如图所示。则下列关于各物质状态的说法正确的是( )

A.A、B、C、D都是气体
B.C、D都是气体,A、B中有一种是气体
C.A、B都不是气体,C、D中有一种是气体
D.A、B都是气体,C、D中有一种是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的Na2CO3、NaHCO3组成的混合物溶于水,配成1L溶液,取出50ml溶液,然后用0.05mol/L盐酸与它反应,得到图象如下(已知:1mol=1000mmol)
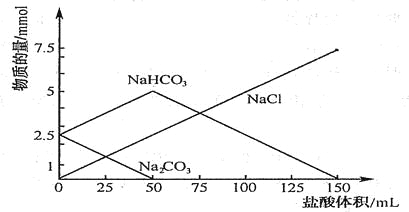
(1)盐酸加到25ml时溶液中发生反应的化学方程式 .
(2)原混合物中Na2CO3物质的量为 mol
(3)盐酸加到150ml时,放出标准状况下气体 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式 。
(2)写出NaClO3发生反应的主要离子方程式 ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 。
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为 。
(4)“操作1”中包含3个基本实验操作,它们依次是 、 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是 。
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是 ;其使用的最佳pH范围是 。
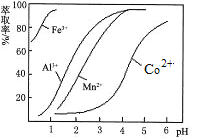
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 。(答一条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com