
【题目】下列化学用语中正确的是
A.NH4HCO3溶液中加入足量的NaOH浓溶液:NH4+ + OH- = NH3↑ + H2O
B.向FeBr2溶液中滴加少量氯水:2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
C.用电子式表示HCl的形成过程:![]()
D.硫磺在空气中燃烧:2S + 3O2 ![]() 2SO3
2SO3
科目:高中化学 来源: 题型:
【题目】新型无机非金属材料中,氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:

请回答下列问题:
(1) 由B2O3制备BN的化学方程式是_________________________________;
(2) 基态B原子的电子排布图为________________;B和N相比,电负性较大的是__________,BN中B元素的化合价为__________;
(3) 在BF3分子中,F—B—F的键角是________, B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF-4的立体构型为________;
(4) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为___________________,层间作用力为________;
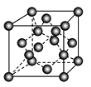
(5) 六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm,立方氮化硼的一个晶胞中含有______个氮原子、________个硼原子,立方氮化硼的密度是________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA,右图为金刚石晶胞)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示4个碳原子相互结合的方式。小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合。

(1)图中属于烷烃的是_________(填字母)。
(2)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成_____和______;不仅可以形成___________,还可以形成碳环。
(3)上图中互为同分异构体的是:A与_________;B与_________;D与_______(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了A~R 9种元素在周期表中的位置:

(1)F元素的名称为 ;画出B的原子结构示意图: 。
(2)这9种元素中,化学性质最不活泼的是_______;既具有非金属元素的某些性质,又可能具有金属元素的某些性质的元素是 。(填元素符号)
(3)A、D、E三种元素的最高价氧化物形成的晶体中属于分子晶体的是 ,A、B两元素的氧化物中熔点较高的是 ,C、D、F形成的氢化物分子中共价键的极性由强到弱的顺序为 。(填化学式)
(4)工业上用D的一种单质为原料生产E单质粗品的化学方程式为 。
(5)G和H的原子序数相差 。(填数字)
(6)写出一个能证明G比H活泼的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、Q、X、Y、Z是原子序数依次增大的五种短周期元素,R与Q形成的气态化合物,在标准下的密度为0.76 g/L,X、Y、Z三种元素族序数之和为10,Y是地壳中含量最多的金属元素,Y单质能强碱溶液反应,Z元素原子最外层电子数是电子层数的两倍。
(1)X在周期表中的位置 ;X、Y、Z三种元素形成的简单离子半径由大到小的顺序是 。(用离子符号回答)
(2)X和R两种元素按原子个数比1:1组成的化合物的电子式为 ,推测这种化合物具有较强的 。(填“氧化性”或“还原性”)
(3)写出Y、Z两种元素最高价氧化物对应的水化物相反应的离子方程式: 。
(4)水的沸点远高于Z元素的氢化物的沸点,原因是 。
(5)Q4是一种Q元素的新单质,可用作推进剂或炸药,推算其分子中含有 对共用电子。
(6)由R、Q两元素组成的一种液态化合物W常用作还原剂,W分子中含有18个电子,W分子的结构式为 。W与氢氧化铜悬浊液反应生成氧化亚铜,同时产生一种稳定的气态单质,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表:


请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)____________________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A 的反应液中,目的是____________________;当试管A内的主要反应完成后温度计水银球的位置应在略低于试管A 的支管口处,目的是____________________
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,烧杯B内盛装的液体可以是____________(在题给物质中找);
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。该方案为_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中A试管盛有无水乙醇(沸点为78℃),B处为螺旋状的细铜丝,C处为无水硫酸铜粉末,干燥管D中盛有碱石灰,E为新制的氢氧化铜,F为氧气的发生装置。

(1)在实验过程中,需要加热的仪器(或区域)有(填仪器或区域的代号A~F)______。
(2)B处发生的化学反应方程式为______ 。
(3)C处应出现的现象是 ,
D处使用碱石灰的作用是 ,
E处应出现的实验现象是 ,
F处可以添加的固体药品是 。
(4)若本实验中拿去F装置(包括其上附的单孔塞和导管),同时将A试管处原来的双孔塞换成单孔塞用以保证装置的气密性,其它操作不变,则发现C处无明显变化,而E处除了依然有上述(3)中所出现的现象之外,还有气体不断地逸出.由此推断此时B处发生反应的化学方程式为______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)莽草酸是合成治疗禽流感的药物——达菲的原料之一。莽草酸是A的一种同分异构体,A的结构简式为

回答下列问题:
(1)A的分子式为 。
(2)A可能发生的化学反应有 。(填编号)
①能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②可发生酯化反应
③可与氢氧化钠溶液发生中和反应
④可与金属钠发生置换反应
⑤在铜或银的催化作用下,可被空气中的氧气氧化
(二)乙醇在能源、生产及日常生活等许多方面都有十分广泛的应用。请计算:
(1)将足量乙醇与9.2g金属钠充分反应,则标准状况下生成气体的体积是 L。
(2)若一定量的乙醇和O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物依次经过浓硫酸和碱石灰使其被充分吸收,浓硫酸增重10.8g,碱石灰重13.2g。求氧气的的物质的量是 mol,燃烧产物的平均摩尔质量是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶。Cr2O72-+3C2H5OH+16H+=4[Cr(H2O)6]3++3CH3COOH
(1)铬原子核外有______个未成对电子。1mol[Cr(H2O)6]3+中含有δ键的数目是______。
(2)CH3COOH中C原子轨道杂化类型为_________。
(3)CH3CH2OH与H2O可以任意比互溶,是因为_________。
(4)C、O位于周期表中第二周期,请比较两者第一电离大小:C_____O(填“>”或“<”)
(5)Cr和Ca可以形成一种具有特殊导电性的复合氧化物,晶胞如图所示。该晶体的化学式为__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com