
(4分)已知1mol H2燃烧生成液态水放出热量为285.8kJ,C2H4、C2H6各1mol分别燃烧生成液态水和CO2,放出热量分别为1409.5kJ、1558kJ。试写出C2H4生成C2H6的热化学方程式 。

C2H4(g)+H2(g)=C2H6(g) △H=-137.3kJ/mol
【解析】
试题分析:根据已知信息可知,氢气、乙烯和乙烷燃烧的热化学方程式分别是①H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8kJ/mol;②C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) ΔH=-1409.5kJ/mol;③C2H6(g)+7/2O2(g)=2CO2(g)+3H2O(l) ΔH=-1558kJ/mol。所以根据盖斯定律可知,①+②-③即得到C2H4(g)+H2(g)=C2H6(g),所以该反应的反应热△H=-285.8kJ/mol-1409.5kJ/mol+1558kJ/mol=-137.3kJ/mol。
考点:考查盖斯定律的应用和反应热的计算
点评:该题是高考中的常见考点,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固与训练,有助于培养学生的逻辑推理能力和应试能力,提高学生的学习效率。该题的关键是准确写出有关反应的热化学方程式,然后根据盖斯定律直接列式计算即可。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
 (2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
(2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
| ||
| △ |

| c2(SO3) |
| c2(SO2)c(O2) |
| c2(SO3) |
| c2(SO2)c(O2) |
| 实验次数 | 铵盐质量(g) | 浓硫酸增加的质量(g) |
| 第一次 | 1.570 | 0.340 |
| 第二次 | 3.140 | 0.680 |
| 第三次 | 4.710 | 0.510 |
| 第四次 | 6.280 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:


| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |






查看答案和解析>>
科目:高中化学 来源: 题型:

| 醇 |
| △ |
| 醇 |
| △ |
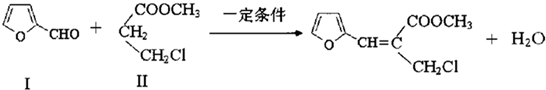
 )也能与化合物Ⅳ发生Knoevenagel反应,则其生成物的结构简式为
)也能与化合物Ⅳ发生Knoevenagel反应,则其生成物的结构简式为

 (任写一种)
(任写一种) (任写一种)
(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:

| 乙醇 |
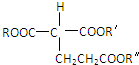
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
| 醇 |
| △ |
| 醇 |
| △ |


 等
等 等
等

查看答案和解析>>
科目:高中化学 来源: 题型:
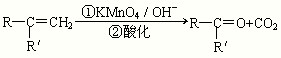 (R、R'可表示烃基或官能团)
(R、R'可表示烃基或官能团)
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com