
【题目】指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
(1)石蕊试纸(检验气体):________;
(2)容量瓶:________;
(3)酸式滴定管:________;
(4)集气瓶(收集氯化氢):________。
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】下列关于二氧化硅的叙述不正确的是
A.二氧化硅晶体是由SiO2分子构成的,它的熔点高,硬度大
B.不可用石英坩埚熔融烧碱
C.二氧化硅可用于制造石英钟表的压电材料和光导纤维
D.二氧化硅能溶于氢氟酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(C6H10O5)n![]() C6H12O6
C6H12O6![]() CH2OH(CHOH)4COOH。 下列说法正确的是( )
CH2OH(CHOH)4COOH。 下列说法正确的是( )
A. (C6H10O5)n和C6H12O6互为同系物
B. 反应②属于加成反应
C. 向①反应后的溶液中直接滴加银氨溶液并加热,可验证C6H12O6的生成
D. 1 mol CH2OH(CHOH)4COOH最多消耗6 molNa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ写出下列化学反应方程式 :①苯的硝化反应: ________ ②淀粉水解的化学方程式: __________
Ⅱ写出下列物质的电子式 :CaCl2________;HClO________;Na2O2________;CO2________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1 NaOH溶液,实验尚缺少的玻璃用品是___________、___________。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒___________(填“能”或“否”),其
原因是 。
(3)他们记录的实验数据如下:

已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。
①计算完成上表ΔH=_____________。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果__________(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果____________(填“有”或“无”)影响。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色溶液中大量共存的一组离子是
A. Cu2+、SO42—、OH—、K+ B. Fe3+、NO3—、Cl—、H+
C. K+、CO32—、Cl—、H+ D. H+、Na+、Cl—、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不锈钢表面用硝酸和氢氟酸的混酸处理后,产生的酸洗废液中含有Fe3+、Ni2+、NO3-、F-和+6价铬的含氧酸根离子等.如图是综合利用该酸洗废液的工艺流程:
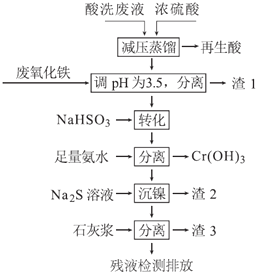
已知:
①金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
②Ni2+与足量氨水的反应为:Ni2++6NH3[Ni(NH3)6]2+
(1)再生酸中含有______,采取减压蒸馏的原因是______(用化学方程式表示).
(2)利用废氧化铁(主要成分为Fe2O3)代替烧碱调节pH的好处是______.
(3)请写出“转化”时NaHSO3与Cr2O72-发生反应的离子反应方程式:______.
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为:______.
(5)滤渣3的主要成分为Ca(OH)2和_________________________.
(6)经检测,最后的残液中c(Ca2+)=0.004molL-1,则残液中F-浓度为______mgL-1,[已知Ksp(CaF2)=4×10-11mol3L-3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 不溶于水的银盐见光都能分解
B. AgBr见光分解,可制作感光材料
C. AgI可用于人工降雨
D. AgCl、AgBr和AgI既不溶于水也不溶于酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com