
某有机物分子中含有下列基团:2个 、2个-CH2-、3个-CH3和一个-COOH,该有机物可能的结构有(不考虑立体异构)( )
、2个-CH2-、3个-CH3和一个-COOH,该有机物可能的结构有(不考虑立体异构)( )
A.8种 B.9种 C.10种 D.11种
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
已知1~18号元素的离子aX m+、bY n+、cZP-、dWk-都具有相同的电子层结构,下列关系正确的是
A.若P>K,则还原性cZP- <dWk-
B.若m > n, 则碱性 X(OH)m > Y(OH)n
C.若半径aX m+>bY n+ ,则a<b
D.若半径aX m+ > bY n+ ,则X的单质一定能从含Y n+ 的盐溶液中置换出Y
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是
A.H2S、H2O、HF的稳定性依次增强
B.RbOH、KOH、Mg(OH)2的碱性依次减弱
C.Ca、Mg、Na的还原性依次减弱
D.H2SiO3、H2CO3、H2SO4的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在研究化学反应中的能量变化时,做了下面的实验:

在一个小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据实验步骤,填写下表,并回答问题。
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 ① 产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 ③ 生成 |
① ② ③
④写出实验过程中发生反应的化学方程式:____________________。
⑤实验中要立即用玻璃棒迅速搅拌的原因是: __________________。
⑥在上述实验过程中,为什么用浸有稀硫酸的湿棉花置于多孔塑料板上?
______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
 元素周期表中铋元素的数据见右图,下列说法不正确的是( )。
元素周期表中铋元素的数据见右图,下列说法不正确的是( )。
A.Bi原子s轨道的形状是球形的,p轨道的形状是纺锤形
B.Bi元素的相对原子质量是209.0
C.Bi原子6p能级中6px、6py、6pz轨道上各有一个电子
D.Bi原子最外层有5个能量相同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质提纯的方法正确的是( )
| 选项 | 待提纯物质 | 杂质 | 主要操作方法 |
| A | 溴苯 | 苯 | 加入铁粉和溴,过滤 |
| B | 碘水 | 水 | 用酒精萃取碘水中的碘 |
| C | 乙烷 | 乙烯 | 通入酸性高锰酸钾溶液,洗气 |
| D | 碘化钾 | 淀粉 | 多次渗析 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有关物质的结构和组成如图所示,下列说法中不正确的是 ( )
|
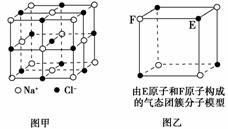
A.在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体
B.该气态团簇分子(图乙)的分子式为EF或FE
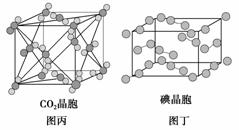
C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D.在碘晶体(图丁)中,碘分子的排列有两种不同的方向
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱 原理制取Na2CO3的流程图。
原理制取Na2CO3的流程图。

已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序是a→________→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣 b.加入盐 酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是_________________________ _________________________________________________________________。
(2)灼烧固体A制Na2CO3在________(填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是_____________________________________ _________________________________________________________________。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3使pH降低,反应的离子方程式为____________________。
(3)下图装置中常用于实验室制备CO2的是________(填字母编号);用b装置制备NH3,分液漏斗中盛放的试剂是________(填试剂名称),烧瓶内可加入的固体试剂是________(填试剂名称)。

(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。(仪器自选)请把实验方案填全:
供选择的试剂:1.0 mol·L-1 H2SO4 溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g天然碱晶体样品,溶于适量蒸馏水中。
②_______________________________________________________________。
③_______________________________________________________________。
④计算天然碱晶体中含Na2CO3的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明氯元素比硫元素非金属性强的是 ( )
①HCl比H2S稳定;②HClO4酸性比H2SO4强;③Cl2能与H2S反应生成S;④Cl原子最外层有7个电子,S原子最外层有6个电子;⑤Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS;⑥盐酸是强酸,而氢硫酸是弱酸
A.①②③④⑤⑥ B.①②③④⑥ C.①②③⑤ D.②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com