
分析 发生反应:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+H2O,根据n=$\frac{m}{M}$计算二氧化锰的物质的量,根据方程式计算氯气的物质的量,被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl的物质的量.
解答 解:4.35g二氧化锰的物质的量=$\frac{4.35g}{87g/mol}$=0.05mol
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+H2O
1 4 1
0.05mol $\frac{100g×36.5%}{36.5g/mol}$ x
因为:$\frac{1}{4}>\frac{0.05}{1}$,所以盐酸过量,二氧化锰完全反应,
x=$\frac{0.05mol×1}{1}$=0.05mol
(1)生成氯气的质量=0.05mol×71g/mol=3.55g,
(2)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl的物质的量=2×0.05mol=0.1mol,
答:(1)生成氯气的质量为3.55g;
(2)被氧化的HCl的物质的量为0.1mol.
点评 本题考查化学方程式的有关计算、氧化还原反应计算,比较基础,注意对基础知识的理解掌握.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | H2SiO3$\stackrel{△}{→}$SiO2$\stackrel{HCI(aq)}{→}$SiCl4 | |
| B. | 饱和食盐水$\stackrel{NH_{3}•CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | Na$\stackrel{O_{2}/△}{→}$Na2O2$\stackrel{HI(aq)}{→}$NaI | |
| D. | Cu2(OH)2CO3$\stackrel{H_{2}SO_{4}}{→}$CuSO4(aq)$\stackrel{Na}{→}$Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
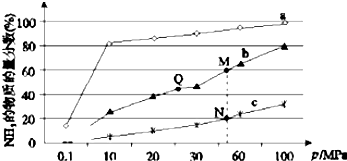
| A. | 上图中M、N、Q点平衡常数K 的大小关系为K(M)=K(Q)>K(N) | |
| B. | 加催化剂能加快反应速率但H2的平衡转化率不变 | |
| C. | 相同压强条件下,投料相同,达到平衡所需时间关系为a>b>c | |
| D. | 由曲线a可知,当压强增加到10OMPa以上,NH3的物质的量分数可达到100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于2amol•L-1 | B. | 等于2amol•L-1 | C. | 小于2amol•L-1 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
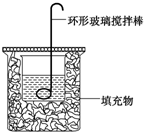 某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.
某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
| 3 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 +NaOH→
+NaOH→ +
+
 +HCl→
+HCl→

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 物质 | 正丁醇 | 正溴丁烷 |
| 沸点/℃ | 117.2 | 101.6 |
| 熔点/℃ | -89.12 | -112.4 |
| 密度/g•cm-3 | 0.8098 | 1.2758 |
| 溶解性 | 微溶于水,溶于浓硫酸 | 不溶于水和浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com