
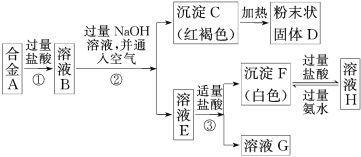
【题目】已知合金A由两种常见金属组成。为测定其组成,某同学的实验流程如图所示:
请回答:
(1)过程②中分离C和E的化学实验基本操作是________________________;
(2)溶液H中所含的阳离子有________________(用离子符号表示);
(3)合金A与D在高温下反应的化学方程式_____________________________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q是原子序教依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体, X、Y、W在周期表中的相对位里关系如图.下列说法正确的是
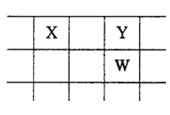
A. 五种元素中,原子半径最大的是W
B. Y的氢化物的沸点比W的氢化物的沸点低
C. Y与Z 形成的化合物都可以和盐酸反应
D. Z与Q形成的化合物的水解液一定显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届天津市五区县上学期期末联考】下列有关物质的性质与用途说法不正确的是
A.FeCl3易溶于水,可用作净水剂
B.硅是半导体材料,纯净的硅是光纤制品的基本原料
C.浓硫酸能干燥氯气,说明浓硫酸具有吸水性
D.氨易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有两瓶温度分别为15℃和35℃,pH均为1的H2SO4溶液,两溶液的物理量相等的为
A.c(H+) B.c(OH-)
C.KW D.水电离的氢离子浓度c水(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com