
| A.Ba(OH)2溶液与稀硫酸 |
| B.Cu(OH)2与稀硫酸 |
| C.NaOH溶液与稀硫酸 |
| D.NH3?H2O与稀硫酸 |
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源:不详 题型:填空题
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无现象 |
| ② | B+D | 有气体放出 |
| ③ | C+B | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4+ | B.Mg2+ | C.Fe2+ | D.Al3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
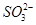 之间发生怎样的反应,请你一起参与并协助他们完成实验。(1)提出猜想:
之间发生怎样的反应,请你一起参与并协助他们完成实验。(1)提出猜想: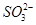 +6H2O===2Fe(OH)3(胶体)+3H2SO3。
+6H2O===2Fe(OH)3(胶体)+3H2SO3。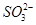 水解能力较
水解能力较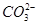 小外,还有_ _______。
小外,还有_ _______。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.向NaAlO2溶液中滴入HCl至过量 |
| B.向澄清石灰水中通入CO2至过量 |
| C.向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量 |
| D.向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至沉淀消失 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在pH=1的溶液中,Cu2+、Fe2+、NO3-和SO42-能大量共存 |
| B.用惰性电极电解饱和氯化钠溶液的离子方程式:2Cl- + 2H+ = H2↑+ Cl2↑ |
| C.镁铝合金被碱液腐蚀时,负极反应式为:Mg — 2e- = Mg2+ |
| D.检验某未知溶液中是否含SO42-时,应先加盐酸酸化,再加BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com