
【题目】Fe2+、Fe3+与O![]() 、CN-、F-有机分子等形成的化合物具有广泛的应用。
、CN-、F-有机分子等形成的化合物具有广泛的应用。
(1)C、N、O原子的第一电离能由大到小的顺序是___________________________。
(2)Fe2+基态核外电子排布式为__________________________。
(3)乙酰基二茂铁是常用汽油抗震剂,其结构如图1所示。
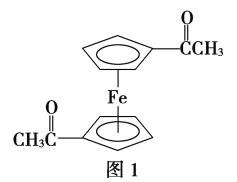
此物质中碳原子的杂化方式是______________________。
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为________________。已知(CN)2是直线型分子,并具有对称性,则(CN)2中π键和σ键的个数比为___________________________。
(5)F-不仅可与Fe3+形成[FeF6]3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,结构如图2所示。
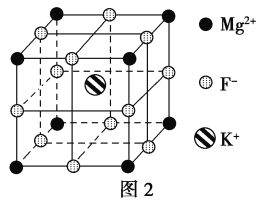
该晶体的化学式为_________________________。
【答案】(1)N>O>C (2)1s22s22p63s23p63d6(或[Ar]3d6)
(3)sp3、sp2 (4)CO(或N2) 4∶3 (5)KMgF3
【解析】(1)同周期第一电离能自左而右具有增大趋势,所以第一电离能O>C。由于N原子2p能级有3个电子,处于半满稳定状态,能量较低,第一电离能大于相邻元素,所以C、N、O三种元素的第一电离能数值由大到小的顺序为N>O>C。(2)Fe是26号元素,其原子核外电子排布式为[Ar]3d64s2,Fe2+为Fe原子失去4s上2个电子,则Fe2+的核外电子排布式为1s22s22p63s23p63d6或[Ar]3d6。(3)乙酰基二茂铁中甲基碳原子采用sp3杂化,羰基碳原子采用sp2杂化。(4)配合物K3Fe(CN)6的配体为CN-,C得到一个e-为N或N得到一个e-为O,所以CN-与N2或CO互为等电子体;(CN)2为直线型分子,具有对称性,其结构式为NCCN,单键为σ键,CN中含有一个σ键,2个π键,因此(CN)2中π键和σ键的个数比为4∶3。(5)根据晶胞结构可知,Mg2+、F-、K+分别位于顶点、棱心和体心处,根据均摊法可知,晶胞中含有的Mg2+、F-、K+个数分别是8×![]() =1个,12×
=1个,12×![]() =3个,1个,所以该物质的化学式为KMgF3。
=3个,1个,所以该物质的化学式为KMgF3。


科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中:NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是 (用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH4+) (填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH4+)。
(3)如图是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
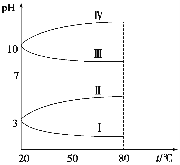
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是 (填写字母),导致pH随温度变化的原因是 ;
②20 ℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)= 。
(4)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
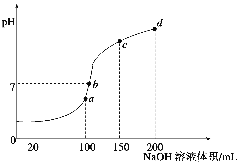
试分析图中a、b、c、d四个点,水的电离程度最大的是 ;在b点,溶液中各离子浓度由大到小的排列顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的正确判断的是
A.在pH= 12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存
B.在pH =0的溶液中,Na+、NO3-、SO32-、K+可以常量共存
C.由0.l mol/L一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH![]() B++OH-
B++OH-
D.pH =2的一元酸和pH =12的一元强碱等体积混后溶液一定存在:c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离或提纯物质的方法正确的是( )
A.用酒精萃取碘水中的碘
B.用蒸馏法进行海水淡化
C.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
D.用加热﹣蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)元素的第一电离能:N________O(填“>”或“<”)。
(2)基态Fe2+的电子排布式为___________________________。
(3)在N、Mg、Al、Si四种元素中,有一种元素的电离能数据如下:
电离能 | I1 | I2 | I3 | I4 | … |
In/kJ·mol-1 | 578 | 1 817 | 2 745 | 11 575 | … |
则该元素的元素符号是________。
(4)NO![]() 的空间构型_____________________(用文字描述),SO
的空间构型_____________________(用文字描述),SO![]() 中硫原子的杂化方式为________________________。
中硫原子的杂化方式为________________________。
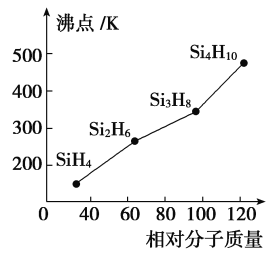
(5)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是_______________________。
(6)金属铜原子的堆积方式为面心立方最密堆积,铜的原子半径为r nm,则铜晶胞的体积表达式为________ cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①烧杯,②蒸发皿,③烧瓶,④试管,⑤坩埚,⑥锥形瓶,⑦容量瓶,⑧集气瓶,⑨量筒,⑩表面皿 其中可以用酒精灯直接加热的仪器为( )
A. ①②③④⑤⑥⑦⑧⑨⑩ B. ①②③④⑤⑥ C. ②④⑤ D. ①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F原子基态的核外电子排布式为_____________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点远高于元素A的简单气态氢化物的沸点,其主要原因是______________________________。
(4)由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-的结构式为___________________________。
(5)在元素A与E所形成的常见化合物中,A原子轨道的杂化类型为________。
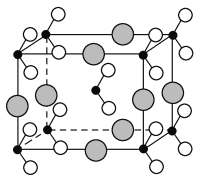
(6)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
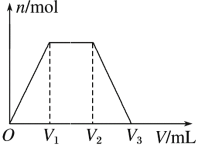
【题目】常温下,有KOH和Ca(OH)2的混合溶液,测得其pH=13。取此溶液300 mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示,图中V1为224 mL(标准状况),则图中V2、V3的数值(单位为mL)分别是( )
A.336、672 B.448、672
C.1120、1176 D.296、352
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com