
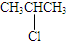 ③
③ ④
④ .
.分析 (1)含有醛基的物质能与银氨溶液反应;
(2)甲苯与浓硝酸反应生成TNT;
(3)苯酚与甲醛缩聚形成酚醛树脂;
(4)卤代烃在氢氧化钠醇溶液、加热条件下发生消去反应.
解答 解:(1)能与银氨溶液反应生成丙酸铵的是 CH3CH2CHO,故答案为:①;
(2) 与浓硝酸反应生成TNT,故答案为:④;
与浓硝酸反应生成TNT,故答案为:④;
(3) 与甲醛发生缩聚反应形成酚醛树脂,故答案为:③;
与甲醛发生缩聚反应形成酚醛树脂,故答案为:③;
(4)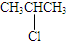 在氢氧化钠醇溶液、加热条件下发生消去反应,反应方程式为:CH3CHClCH3+NaOH$→_{△}^{醇}$CH3CH=CH2↑+NaCl+H2O,
在氢氧化钠醇溶液、加热条件下发生消去反应,反应方程式为:CH3CHClCH3+NaOH$→_{△}^{醇}$CH3CH=CH2↑+NaCl+H2O,
故答案为:CH3CHClCH3+NaOH$→_{△}^{醇}$CH3CH=CH2↑+NaCl+H2O.
点评 本题考查有机物的结构与性质,比较基础,旨在考查学生对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-6mol•L-1 | |
| B. | pH相等的①NH4C1、②(NH4)2SO4、③NH4HSO4三种溶液中,c(NH4+)大小顺序为:①=②>③ | |
| C. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
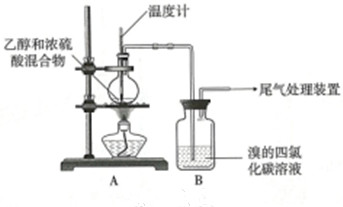
| 操作 | 现象 |
| 点燃酒精灯, 加热至170℃ | a.A中烧瓶内液体渐渐变黑 b.B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕 | c.A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环乙醇 | 0.96 | 25.93 | 161 | 能溶于水 |
| 环乙烯 | 0.81 | -103 | 83 | 难溶于水 |
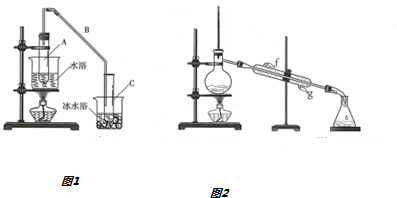
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiC | B. | SiO2 | C. | Si | D. | Si3N4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,含等质量氧元素的NO和CO的体积相等 | |
| B. | NO是一种有刺激性气味的红棕色气体 | |
| C. | NO易溶于水,所以可用排空气法收集 | |
| D. | NO不能通过化合反应获得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定不存在的离子是Mg2+、Ba2+,不能确定是否含有K+、NO3- | |
| B. | 一定存在的离子是CO32-、SO42-,CO32-的物质的量浓度为0.25mol•L-1,SO42-的物质的量浓度为0.1mol•L-1 | |
| C. | 一定存在的离子是CO32-、SO42-、K+,其中K+浓度≥0.2mol•L-1 | |
| D. | 一定存在的离子是CO32-、SO42-、K+,其中K+浓度为0.2mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com