
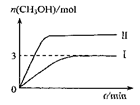
Ϊ��СCO2�Ի�����Ӱ�죬�ڳ�������̼����ͬʱ�������ǿ��CO2�������õ��о�����T10C ʱ����9molCO2��12molH2����3L�ܱ������У�������ӦCO2(g)+3H2(g) 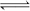 CH3OH(g)+H2O(g) ��H <0��������CH3OH�����ʵ�����ʱ��仯����ͼ����I��ʾ��ƽ��ʱ������ѹǿΪP���ı�ijһ�������½���������Ӧ��CH3OH�����ʵ�����ʱ��仯����ͼ����II��ʾ������˵����ȷ����
CH3OH(g)+H2O(g) ��H <0��������CH3OH�����ʵ�����ʱ��仯����ͼ����I��ʾ��ƽ��ʱ������ѹǿΪP���ı�ijһ�������½���������Ӧ��CH3OH�����ʵ�����ʱ��仯����ͼ����II��ʾ������˵����ȷ����
A������II��Ӧ�������ı��Ǽ�Сѹǿ
B����T2��Cʱ��������Ӧƽ�ⳣ��Ϊ0.42����T2< T1
C����T10Cʱ������ʼʱ�������г���5 mol CO2��5 mol H2��5 mol CH3OH(g)�� 5 mol H2O(g)�����ƽ��ǰv(��)>v(�棩
D����T10Cʱ������ʼʱ�������г���4.5molCO2��6mol H2 ��ƽ��ʱ������ѹǿ


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ����������ԭ��Ӧ���ǣ�������
| �� | A�� | Cu+4 HNO3��Ũ���TCu��NO3��2+2 NO2��+2 H2O |
| �� | B�� | 3O2�T2O3�� |
| �� | C�� | HCl+NaHCO3=NaCl+H2O+CO2 |
| �� | D�� | CuCl2+2NaOH=Cu��OH��2+2NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1mol��ϩ(C2H4)��������ȫ�ӳɺ���������ȡ����������������������� ��
A��7mol�� �� B��6mol�� ��C��5mol�� D��4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1molSO2��1molO2ͨ��һ�ݻ�������ܱ������У���һ���¶Ⱥʹ��������·�����Ӧ SO2(g)+ 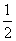 O2(g)
O2(g)  SO3(g)���ﵽƽ���SO3Ϊ0.3mol����ʱ������0.5molSO2��0.5mol O2�������´ﵽƽ���SO3���ʵ���Ϊ
SO3(g)���ﵽƽ���SO3Ϊ0.3mol����ʱ������0.5molSO2��0.5mol O2�������´ﵽƽ���SO3���ʵ���Ϊ
A������0.3mol B������0.15mol
C����0.15mol D������0.15mol����0.3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��HCN(aq)�� NaOH(aq) ==NaCN(aq)��H2O(l) ��H����12.1 kJ��mol��1��
HCl(aq)��NaOH(aq) ==NaCl (aq)��H2O(l) ��H����55.6 kJ��mol��1
��HCN��ˮ��Һ�е���Ħ�H����
A����43.5 kJ��mol��1�������������������� B ����67.7 kJ��mol��1
���43.5 kJ��mol��1 ��������������������D����67.7 kJ��mol��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
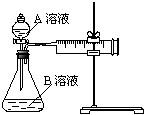 �̲���������KMnO4��H2C2O4�����ᣩ��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ����ӷ���ʽΪ��2MnO4����5H2C2O4��6H����2Mn2����10CO2����8H2O��һʵ��С����ͨ���ⶨ��λʱ��������CO2�����ʣ�̽��ij��Ӱ�컯ѧ��Ӧ���ʵ����أ����ʵ�鷽�����£�KMnO4��Һ���ữ����
�̲���������KMnO4��H2C2O4�����ᣩ��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ����ӷ���ʽΪ��2MnO4����5H2C2O4��6H����2Mn2����10CO2����8H2O��һʵ��С����ͨ���ⶨ��λʱ��������CO2�����ʣ�̽��ij��Ӱ�컯ѧ��Ӧ���ʵ����أ����ʵ�鷽�����£�KMnO4��Һ���ữ����
| ʵ����� | A��Һ | B��Һ |
| �� | 20 mL 0.1 mol��L��1 H2C2O4��Һ | 30 mL 0.01 mol��L��1 KMnO4��Һ |
| �� | 20 mL 0.2 mol��L��1 H2C2O4��Һ | 30 mL 0.01 mol��L��1 KMnO4��Һ |
 ��д����������ˮ�ĵ��뷽��ʽ�� ��
��д����������ˮ�ĵ��뷽��ʽ�� ��
�Ƹ�ʵ��̽������ ���ضԻ�ѧ��Ӧ���ʵ�Ӱ�졣��ͬʱ������Ͳ������CO2�������С��ϵ�ǣ��� �ڣ����������������
����ʵ�����2 minĩ�ռ���4.48 mL CO2����״���£�����
��2 minĩ�� c(MnO4��)�� mol/L��
�ȳ�ͨ���ⶨһ��ʱ����CO2��������ȽϷ�Ӧ���ʣ���ʵ�黹��ͨ���ⶨ ���Ƚϻ�ѧ��Ӧ���ʡ�
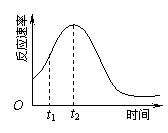
��С��ͬѧ���ַ�Ӧ������ʱ��仯����ͼ��ʾ������t1��t2ʱ�������ʱ�����Ҫԭ������ǣ��ٸ÷�Ӧ���ȣ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������������ɢϵ�ı��������� ( )
A������ķ�ɢ������������ֽ
B�������ܲ������������
C������ķ�ɢ������ֱ����1��100 nm֮��
D�������Ǵ����������ɢϵ�ǻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����5ƿ����ҺA��B��C��D��E ���ɷ־���HCl��BaCl2��NaHSO4��Na2CO3��AgNO3�е�һ�֡���֪��
�� A��B��Ӧ���������� �� B��C��Ӧ�г�������
�� C��D��Ӧ�г������� �� D��E��Ӧ�г�������
�� A��E��Ӧ���������� �� �ڢں͢۵ķ�Ӧ�����ɵij�����ͬһ������
����գ�
��1���ڢں͢۵ķ�Ӧ�У����ɵij������ʵĻ�ѧʽ������ʽ����ͬ���� ��
��2��A�� �� C�� ��E�� ��
��3��A��E��Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪298Kʱ��H+��aq��+OH����aq���TH2O��l����H=��57.3kJ•mol��1���Ʋ⺬1mol HCl��ϡ��Һ�뺬1mol NH3��ϡ��Һ��Ӧ�ų���������������
| �� | A�� | С��57.3 kJ | B�� | ����57.3 kJ | C�� | ����57.3 kJ | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com