
【题目】根据要求回答问题:
(1)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是(填“增大”“减小”或“不变”,下同),ΔH的变化是。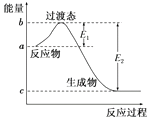
(2)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为。
(3)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1 , 则甲醇蒸气燃烧为液态水的热化学方程式为。
(4)在微生物作用的条件下,NH 经过两步反应被氧化成NO 。这两步的能量变化如图: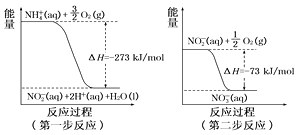
第二步反应是反应(填“放热”或“吸热”)。1 mol NH4+(aq)全部氧化成NO (aq)的热化学方程式是。
【答案】
(1)减小,不变
(2)2Cl2(g)+ TiO2(s)+2C(s)=TiCl4(l)+2CO(g) ΔH=?85.6 kJ·mol?1
(3)CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-764.7 kJ·mol-1
(4)放热,NH 4+ (aq)+ ![]() O2(g)=NO 2- (aq)+2H+(aq)+H2O(l) ΔH=-273 kJ/mol
O2(g)=NO 2- (aq)+2H+(aq)+H2O(l) ΔH=-273 kJ/mol
【解析】(1)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响。E1的变化是减小,ΔH的变化是不变;
(2)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体HCl和一种易水解成TiO2·xH2O的液态化合物TiCl4(l),放热4.28 kJ,反应方程式为2Cl2(g)+ TiO2(s)+2C(s)=TiCl4(l)+2CO(g),0.1 mol Cl2反应放热4.28 kJ,2 mol Cl2反应放热4.28 kJ×2/0.1=85.6 kJ,该反应的热化学方程式为2Cl2(g)+ TiO2(s)+2C(s)=TiCl4(l)+2CO(g) ΔH=85.6 kJ·mol1 ;
(3)利用盖斯定律进行计算,①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1,②CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,依据盖斯定律计算(②×3-①×2+③×2)得:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=3×(-192.9 kJ·mol-1)-2×49.0 kJ·mol-1+(-44 kJ·mol-1)×2=-764.7 KJ·mol-1;则甲醇蒸气燃烧为液态水的热化学方程式为:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-764.7 KJ·mol-1;
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,依据盖斯定律计算(②×3-①×2+③×2)得:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=3×(-192.9 kJ·mol-1)-2×49.0 kJ·mol-1+(-44 kJ·mol-1)×2=-764.7 KJ·mol-1;则甲醇蒸气燃烧为液态水的热化学方程式为:CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-764.7 KJ·mol-1;
(4)由图可知,第二步反应反应物能量高于生成物能量,是放热反应;由图可知,第一步热化学反应为NH4+(aq)+1.5O2(g)=2H+(aq)+NO2-(aq)+H2O(l)△H=-273 kJ·mol-1,即1 mol NH 4+ (aq)全部氧化成NO 2- (aq)的热化学方程式。
【考点精析】掌握吸热反应和放热反应是解答本题的根本,需要知道化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是( )
A. 98%的H2SO4物质的量浓度为18.4mol/L ,则49%的H2SO4物质的量浓度为9.2mol/L
B. 当2L水吸收44.8L氨气(标况)时所得氨水的浓度不是1molL-1,只有当44.8L(标况)氨气溶于水制得2L氨水时,其浓度才是1molL-1
C. 只含K2SO4和NaCl的混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同
D. 50mL 1mol/L的AlCl3溶液中的Cl—浓度与50ml 3mol/L的BaCl2溶液Cl—浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇 ![]() 广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )
广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )
A.1 mol 1 mol
B.3.5 mol 7 mol
C.3.5 mol 6 mol
D.6 mol 7 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组用右图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是( )
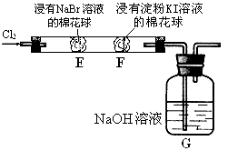
A.E处棉花球变成黄色,说明Cl2的氧化性比Br2强
B.F处棉花球变成蓝色,说明Br2的氧化性比I2强
C.E处发生反应的离子方程式为:Cl2+ 2Br-=2Cl-+ Br2
D.G装置中NaOH溶液与Cl2反应的离子方程式为:2OH- + Cl2 = ClO-+ Cl-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示) , 设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过mol电子。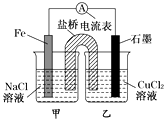
(2)用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式 , 然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO ![]() ,试写出该反应的离子方程式。
,试写出该反应的离子方程式。
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是溶液变红,电极反应为;乙装置中石墨(1)为极(填“正”、“负”、“阴”或“阳”),乙装置中与铜丝相连石墨电极上发生的反应式为。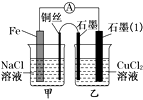
(4)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为、。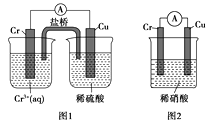
查看答案和解析>>
科目:高中化学 来源: 题型:
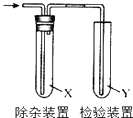
【题目】用如图所示装置检验乙烯时不需要除杂的是( )
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4加热至170℃ | NaOH | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4加热至170℃ | NaOH | Br2的CCl4溶液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚戊二酸丙二醇酯(PPG: ![]() )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下: 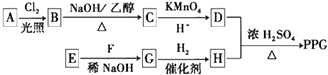
已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢
②化合物B为单氯代烃;化合物C的分子式为C5H8
③E,F为相对分子质量差14的同系物,F是福尔马林的溶质
④R1CHO+R2CH2CHO ![]()
![]() .
.
⑤ ![]()
回答下列问题:
(1)A的结构简式为 .
(2)由B生成C的化学方程式为 .
(3)由E和F生成G的反应类型为 , G的化学名称为 .
(4)由D和H生成PPG的化学方程式为
(5)写出D的同分异构体中能同时满足下列条件的结构简式 .
①与D具有相同种类和数目的官能团
②核磁共振氢谱显示为2组峰,且峰面积比为3:1.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com