
【题目】(1)共建“带一路”符合国际社会的根本利益,彰显人类社会的共同理想和美好追求。
下列贸易商品中,主要成分属于无机物的是______(填标号)

(2)下列有关有机化合物的说法正确的是__________ (填标号,3分)
A.棱晶烷(![]() )与苯互为同分异构体
)与苯互为同分异构体
B.分子式为C8H10的芳吞烃有3种不同的线构
C. ![]() 能发生取代、加成、氧化、水解等反应
能发生取代、加成、氧化、水解等反应
D.丙烯酸(CH2=CHCOOH) 与山梨酸(CH3CH=CHCH=CHCOOH) 为同系物
(3)完全燃烧甲烷和乙烯的混合气体1.12L (标准状况下),生成气体进入足量澄清石灰水中,得到6g沉淀。则混合气体中甲烷和乙烯的体积比为_________(填标号,3分)
A.1:1 B.1:2 C.2:1 D.4 :1
【答案】 B A D
【解析】(1)A、丝绸属于蛋白质,属于有机物,选项A不选;B、水晶主要成分为二氧化硅,属于无机物,选项B选;C、绒棉主要成分为纤维素,属于糖类,为有机物,选项C不选;D、葵花籽油属于油脂,属于有机物,选项D不选。答案选B;(2)棱晶烷、苯分子式均为C6H6,互为同分异构体,选项A正确;B、分子式为C8H10的芳香烃有乙苯、邻二甲苯、间二甲苯、对二甲苯4种不同的结构,选项B错误;C、![]() 能发生取代反应、加成反应、氧化反应但不能发生水解反应,选项C错误;D、丙烯酸(CH2=CHCOOH) 与山梨酸(CH3CH=CHCH=CHCOOH) 相差C3H4不符合若干个CH2,不为同系物,选项D错误。答案选A;(3)白色沉淀6g为碳酸钙的质量,故碳酸钙的物质的量=
能发生取代反应、加成反应、氧化反应但不能发生水解反应,选项C错误;D、丙烯酸(CH2=CHCOOH) 与山梨酸(CH3CH=CHCH=CHCOOH) 相差C3H4不符合若干个CH2,不为同系物,选项D错误。答案选A;(3)白色沉淀6g为碳酸钙的质量,故碳酸钙的物质的量=![]() =0.06mol,n(CO2)=n(CaCO3)=0.06mol,1.12L该气态烃的物质的量=
=0.06mol,n(CO2)=n(CaCO3)=0.06mol,1.12L该气态烃的物质的量=![]() =0.05mol,设甲烷的物质的量为x,乙烯的物质的量为y,则有
=0.05mol,设甲烷的物质的量为x,乙烯的物质的量为y,则有![]() ,解得
,解得![]() ,则混合气体中甲烷和乙烯的物质的量之比为0.04mol:0.01mol=4:1,相同条件下气体的物质的量与体积成正比,故混合气体中甲烷和乙烯的体积比为4 :1。答案选D。
,则混合气体中甲烷和乙烯的物质的量之比为0.04mol:0.01mol=4:1,相同条件下气体的物质的量与体积成正比,故混合气体中甲烷和乙烯的体积比为4 :1。答案选D。


科目:高中化学 来源: 题型:
【题目】下列离子方程式中书写正确的一组是( )
①.制取漂白液的反应原理: Cl2+2OH-=== Cl-+ClO-+ H2O
②.铁粉加入到三氯化铁溶液中: Fe3+ +Fe === 2Fe2+
③.NaHCO3溶液中加入稀盐酸:CO32-+2H+![]() CO2↑+H2O
CO2↑+H2O
④.向澄清石灰水中加入少量小苏打溶液: Ca2++OH-+HCO3-=== CaCO3↓+H2O
⑤.硫酸铝溶液与足量的氨水混合反应: Al3+ + 4OH- === AlO2-+ H2O
⑥.过量氯水与FeCl2溶液作用: 2Fe2++Cl2 ==2 Fe3++2Cl-
A. ①②③ B. ③⑥ C. ①③⑥ D. ①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取氨气并完成喷泉实验
(1)写出实验室制取氨气的化学方程式: 。
(2)收集氨气应使用 法,要制取干燥的氨气可选用 做干燥剂。
(3)如图进行喷泉实验,上部烧瓶已装满干燥的氨气,引发水上喷的操作是 ,该实验的原理是

(4)反应后,烧瓶内的溶液中含有的微粒为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定休积的密闭容器中,充入2molA和1molB,发生如下反应2A(g)+B(g)![]() xC(g) 平衡后,C的体积分数为W%,若维持容器容君和温度不变,0.6molA、0.3molB和1.4molC为起始物质。达到平衡后,C的体形分數也为W%。平衡后若缩小容器体积,C的体和分数C%、混合气体平均相对分子质量(M)、平衡常数(K)和正反应速率[V(正)],随压强(P)的变化,一定符合的是
xC(g) 平衡后,C的体积分数为W%,若维持容器容君和温度不变,0.6molA、0.3molB和1.4molC为起始物质。达到平衡后,C的体形分數也为W%。平衡后若缩小容器体积,C的体和分数C%、混合气体平均相对分子质量(M)、平衡常数(K)和正反应速率[V(正)],随压强(P)的变化,一定符合的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天宫二号空间实验室已于2016 年9月15日22时04分在酒泉卫星发射中心发射成功。请回答下列问题:

(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件。石英玻璃的成分是______(填化学式)
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统。碳纤维复合材料具有重量轻、可设计强度高的特点。碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是_____________。
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性。
① 天宫二号使用的光伏太阳能电池,该电池的核心材料是_____,其能量转化方式为_____。
② 下图是一种全天候太阳能电池的工作原理:

太阳照射时的总反应为V3++ VO2++ H2O=V2++VO2++2H+,则负极反应式为__________;夜间时,电池正极为______(填“a”或“b”)。
(4)太阳能、风能发电逐渐得到广泛应用,下列说法中,正确的是______(填字母序号)。
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(5)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的回收利用,流程如下:

已知溶液pH范围不同时,钒的存在形式如下表所示:
钒的化合价 | pH<2 | pH>11 |
+4价 | VO2+,VO(OH)+ | VO(OH)3- |
+5价 | VO2+ | VO43- |
①加入NaOH调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH后生成沉淀1的反应过程为_______、_______;所得滤液1中,铝元素的存在形式为__________。
②向碱性的滤液1 (V的化合价为+4)中加入H2O2的作用是________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月海底天然气水合物(俗称“可燃冰”)试采成功,这是我国能源开发的一次历史性突破。一定条件下,CH4和CO2都能与H2O形成如下图所示的笼状结构(表面的小球是水分子,内部的大球是CH4分子或CO2分子;“可燃冰”是CH4与H2O形成的水合物),其相关参数见下表。
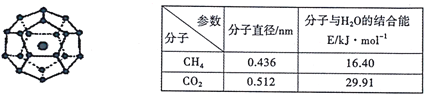
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为_______;碳原子的最高能级的符号是_______,其电子云形状是_______。
(2)CO2分子中碳原子的杂化轨道类型为_______,分子的立体构型为_____。CO2与SO2相同条件下在水中的溶解度较大的是SO2,理由是________。
(3)为开采海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是_______。
(4)“可燃冰”中分子间存在的作用力是氢键和_________,上图中最小的环中连接的原子总数是_______。
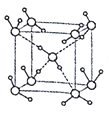
(5)水在不同的温度和压力条件下可形成11种不同结构的晶体,密度从比水轻的0.92g/cm3到约为水的1.5 倍。冰是人们迄今已知的由一种简单分子堆积出结构花样最多的化合物。其中冰- Ⅶ的晶体结构为一个如图所示的立方晶胞,每个水分子与周围4个水分子以氢键结合。设O-H…O距离为apm,阿伏加德罗常数的值为NA,则该冰- Ⅶ晶体的密度为____ g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1 的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是

A. 曲线②代表滴定CH3COOH溶液的曲线
B. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1
C. 在相同温度下,A、B、C三点溶液中水的电离程度: A<C<B
D. D点溶液中:c(Cl-)+ 2c(H+)=2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用容量瓶配制一定物质的量浓度的溶液,回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是______(填仪器名称).

(2)容量瓶上需标有以下6项中的______(填序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线 ⑥酸式或碱式
(3)容量瓶不能______(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(4)在配制过程中,下列操作中能引起误差偏高的有______(填代号).
①未等稀释后的溶液冷却至室温就转移到容量瓶中
②定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
③定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
④定容时,俯视刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com