
(10��)þ���Ͻ��ڽ�ͨ�����ա����ӵ���ҵ���Ź㷺��Ӧ�á�ij��ѧ��ȤС���Զ�þ���Ͻ���Ͻ��л������ã�ʵ���пɽ���ת��Ϊ���������壬��������������������ط�����þ���Ͻ����ת��Ϊ����������ʵ���������£�
�Իش��������⣺
��1����þ���Ͻ��м���NaOH��Һ��д����Ӧ�Ļ�ѧ��Ӧ����ʽ ������B�Ļ�ѧʽ ��
��2�������������ʵ�鲽���У�����Ũ���� �� ��ϴ�ӡ����
��3���������г�����ˮ�Ҵ��Ծ������ϴ�ӣ�ѡ����ˮ�Ҵ���ԭ���� ��
��4������ʼʱ��ȡ��þ���Ͻ���ϵ�����Ϊ9.00 g���õ�����A������Ϊ4.95 g�����������������Ϊ49.95 g������ÿһ����ת���ʾ�Ϊ100%���Ͻ�����в������ڼ�����ʣ������������������Ļ�ѧʽΪ ��
��5��ȡ��������������������ط��������ȷֽ���Ҫ��Ϊ�����Σ�323K-523K��553K-687K��1043K���ϲ���ʧ�أ����ȷֽ��TG������ͼ,
��֪�� ��
��
����ͼʾ���ݼ���ȷ��ÿ���ֽ�IJ��д����һ�ηֽ����Ļ�ѧʽ �������η�Ӧ��ѧ����ʽ ��

��10�֣���1��2Al+2NaOH+2H2O=2NaAlO2+3H2�� (2��) Al(OH)3
��2����ȴ�ᾧ����ᾧ�����֣� ���� ��˳��ߵ������֣�
��3�����پ�����ܽ⣻ϴȥ����������ʣ������ھ���ĸ������2�����ϸ�1�֣���1�㲻���֣�
��4��Al2(SO4)3��18H2O
��5��Al2(SO4)3��3H2O Al2(SO4)3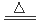 Al2O3+3SO3��(2��)
Al2O3+3SO3��(2��)
��������
�����������1����þ���Ͻ��м���NaOH��Һ��Al������ǿ����Һ������Ӧ����Mg���ܷ�Ӧ���÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��2Al+2NaOH+2H2O=2NaAlO2+3H2�������Թ���A��Mg������Һ��ͨ�������CO2���壬��������H2CO3>Al(OH)3,�ᷢ����Ӧ��NaAlO2+ CO2+2H2O= Al(OH)3��+NaHCO3�����Թ���B��Al(OH)3����2���������ܽ�ù��壬������Ӧ��2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O���õ�����ҺC��Al2(SO4)3��Һ���������ܽ�����¶ȵ����߶��������Դ���Һ�л�þ���ķ���������Ũ������ȴ�ᾧ������ ��ϴ�ӡ������3���������г�����ˮ�Ҵ��Ծ������ϴ�ӣ���ϴȥ������������ӣ�ѡ����ˮ�Ҵ���ԭ���Ǽ��پ�����ܽ⣻ϴȥ����������ʣ������ھ���ĸ����4������ʼʱ��ȡ��þ���Ͻ���ϵ�����Ϊ9.00 g���õ�����A������Ϊ4.95 g������������Ӧ����þ����Ӧ�����ٵ�����Ϊ����������������m(Al)= 9.00 g��4.95 g=4.05 g��n(Al)= 4.05 g��27g/mol=0.15mol�����������������Ϊ49.95 g�������������к���SO42-�����ʵ���Ϊn(SO42-)=3/2n(Al3+)=3/2��0.15mol=0.225mol, Al2(SO4)3��������m(Al2(SO4)3)= (0.15mol��2) ��342g/mol=25.65g�����еĽᾧˮ�����ʵ�����n(H2O)= (49.95 g-25.65g) ��18g/mol=1.35mol����n(Al2(SO4)3)��n(H2O)= (0.15mol��2)��1.35mol=1:18�����Ըýᾧˮ����Ļ�ѧʽ�ǣ�Al2(SO4)3��18H2O��
��5���ڵ�һ���Σ����ٵ�ˮ�������ǣ�m(H2O)=40.54%��49.95 g=20.25 g,ʧȥ�Ľᾧˮ�����ʵ����ǣ�n(H2O)= 20.25 g��18g/mol=1.125mol���ھ�����n(Al2(SO4)3)��n(H2O)= (0.15mol��2): ��1.35mol -1.13mol��=1:3.���Դ�ʱ�õ��ľ���Ļ�ѧʽ��Al2(SO4)3��3H2O���ڵڶ����Σ�ʧȥ�ᾧˮ�����ʵ�����n(H2O)=[ (49.95 g�� 48.65%]��18g/mol=1.35mol���ᾧˮ��ȫʧȥ���õ��Ĺ��������ǣ�Al2(SO4)3�����ڵ������μ��ȷ����ֽⷴӦ�����������ķֽ⣬����ʽ�ǣ�Al2(SO4)3 Al2O3+3SO3����
Al2O3+3SO3����
���㣺����������ȡ��Ӧԭ����֪ʶ����Ҫ����������ȡ�ķ���ʽ����д�������ķ��뷽����������Ŀ�ġ����ʷֽ�ķ�Ӧ�����ȷ����֪ʶ��
��������� ����1�����ʵ��Ʊ� ����2��þ�����仯���� ��������


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015���ɹų���������ظ�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�ε���Һ��ֻ����Na+��Mg2+��Cl-��SO42- �������ӣ�����0��2mol Na+��0��4molMg2+ 0��4molCl-��SO42-�����ʵ���Ϊ
A��0��1mol B��0��3mol C��0��5mol D��0��15mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���ɹų���������ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���û�з�����ѧ��Ӧ����
A���û���̿ȥ�������е���ζ
B�����ȼ�ˮ��������ϲ���������
C���ý��ݹ����������Һ��שͷ����ˮ��
D���ú��轺�����۵���С����ʳƷһ���ܷ��װ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������й��ж���ȷ����

A���������漰�ķ�Ӧ��Ϊ��������ԭ��Ӧ
B����Ӧ�ڲ�������������ҪΪCO32-
C��ʵ��������ɷ�Ӧ��Ӧ���������н���
D����Ӧ�ܵ������ǵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ڹ�ҵ��������
A������������ȼ�����Ȼ��� B���������̺�Ũ���Ṳ��������
C����������ʯ�ҷ�Ӧ��Ư�� D�����NaCl��Һ�ƽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и߶���ѧ����ĩ��ѧ�����ޣ��Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ���ڼӳɷ�Ӧ����
A��CH4+Cl2 CH3Cl+HCl
CH3Cl+HCl
B��CH2=CH2 + HCl CH3CH2Cl
CH3CH2Cl
C��2CH3CH2OH + O2 2CH3CHO+2H2O
2CH3CHO+2H2O
D��2C6H6 + 15O2 12CO2 +6H2O
12CO2 +6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и߶���ѧ����ĩ��ѧ�����ޣ��Ծ��������棩 ���ͣ�ѡ����
���л�ѧ������ȷ����
A������Ľṹ��ʽ��C2H4O2
B�������Ľṹʽ��N N
N
C������ĵ���ʽ��
D����ԭ�ӵĽṹʾ��ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡ��ׯ�и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��7�֣�ij�о���ѧϰС����ȡ�κ���±��Ũ��Һ������K����Mg2����Br����SO42-��Cl���ȣ�����ȡ�ϴ������Ȼ��ؾ��弰Һ�壨Br2��������������������̣�

������������̣��ش�������⣺
��1����������_________����������_________����������_________������������ƣ�
��2����������Ҫ����Ҫ�����������ձ��⣬����Ҫ_________��
��3������������X��Y��Z��Ϊ�˳�ȥ��Һ�е����ʣ�����������BaCl2��Һ ��KOH��Һ�� _____��Һ��
��4��������ɫ��ҺB���Ƿ���SO42���ķ�����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ȥNaCl�к��е�Ca2����Mg2����SO42����HCO3�������ӣ�ͨ�����������Լ�����������Na2CO3 ��BaCl2 ��NaOH ��HCl �ݹ��ˡ������Լ�������������˳����
A���٢ڢۢݢ� B���ۢ٢ݢڢ� C���ۢڢ٢ݢ� D���ܢڢ٢ݢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com