
【题目】品牌膨松剂中发挥作用的物质为碳酸氢钠。某化学兴趣小组利用下列有关装置,加热该膨松剂样品,通过放出气体的量来检验其品质。

(1)装置D仪器的名称是_________。
(2)装置E中所盛试剂为____________,其作用是______________。
(3)装置的连接顺序为_____________(填装置序号)。
(4)实验过程中,装置A中发生反应的化学方程式为________________。
(5)实验过程中必须向装置内通入空气,装置C的作用是除去空气中的________(填化学式)。加热前,通入一段时间空气的具体操作为________________________。
【答案】干燥管 浓硫酸 干燥CO2 CAEBD 2NaHCO3![]() Na2CO3+H2O+CO2↑ CO2 先对装置A、C和E通入一段时间的空气,再连接上装置B、D
Na2CO3+H2O+CO2↑ CO2 先对装置A、C和E通入一段时间的空气,再连接上装置B、D
【解析】
碳酸氢钠不稳定,分解生成二氧化碳和水,可测定水或二氧化碳的质量以判断碳酸氢钠的含量,实验时,应用C装置排出装置内的水、二氧化碳,加热A,生成的水可用E干燥,二氧化碳可用B装置吸收,最后连接D,以免空气中的水、二氧化碳进入B,避免实验误差,根据固体质量的变化,可测得碳酸氢钠的含量,以此解答该题;
(1)由仪器图可知D为干燥管;
答案为:干燥管;
(2)装置E为浓硫酸,可用于干燥二氧化碳;
答案为:浓硫酸;干燥CO2;
(3)由以上分析可知连接的顺序为CAEBD;
答案为:CAEBD;
(4)碳酸氢钠不稳定,加热分解生成碳酸钠、水和二氧化碳,装置A中发生反应的化学方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
答案为:2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(5)装置C的作用是除去空气中的二氧化碳,加热前,通入一段时间空气的具体操作为先对装置A、C和E通入一段时间的空气,再连接上装置B、D;
答案为:CO2;先对装置A、C和E通入一段时间的空气,再连接上装置B、D。


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.9 g D2O中含有的电子数为5NA
B.46 g NO2和N2O4混合气体中含有原子数为3NA
C.1 mol C2H6分子中含共价键总数为6NA
D.7.1 g C12与足量NaOH溶液反应,转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯是一种重要的有机化工原料,其结构简式为![]() ,它一般不可能具有的性质是
,它一般不可能具有的性质是
A. 易溶于水,不易溶于有机溶剂
B. 在空气中燃烧产生黑烟
C. 能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色
D. 能发生加成反应,在一定条件下可与4倍物质的量的氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与对应的结论或解释正确的是
选项 | 操作 | 现象 | 结论或解释 |
A | 用洁净铂丝蘸取某溶液进行焰色反应 | 火焰吴黄色 | 原溶液中有 |
B | 将 | 溶液紫色褪去 |
|
C | 向 | 得到澄清溶液 |
|
D | 向盛有少量溴水的分液漏斗中加入裂化汽油,充分振荡,静置 | 上、下层液体均近无色 | 裂化汽油不可用作溴的萃取溶剂 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是沟通宏观与微观的桥梁。物质的量的计算在生产、生活、科技等方面具有广泛的应用。请回答下列问题。
(1)同温同压下,等质量的CO和CO2,其体积之比为____________。
(2)标准状况下有①44.8LCH4,②9.03×1023个NH3分子,③85gH2S三种气体,对这三种气体的物质的量从大到小的顺序是__________。
(3)一定温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积某化合物,则该化合物的化学式是____________。
(4)某混合盐溶液中含有Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol·L-1、0.25mol·L-1、0.4mol·L-1,则c(SO42-)=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图:电流计的指针会偏转,M极变粗,N极变细符合这种现象的是

A. M是铜,N是锌,R是硫酸溶液
B. M是锌,N是铜,R是硫酸铜溶液
C. M是银,N是锌,R是硝酸银溶液
D. M是铁,N是铜,R是硝酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对烟道气中![]() 进行回收再利用具有较高的社会价值和经济价值。
进行回收再利用具有较高的社会价值和经济价值。
I. ![]() 还原法
还原法

(1)一定条件下,由![]() 和
和![]() 反应生成
反应生成![]() 和
和![]() 的能量变化如图所示,每生成
的能量变化如图所示,每生成![]() ,该反应__________(填“放出”或“吸收”)的热量为____________。
,该反应__________(填“放出”或“吸收”)的热量为____________。
(2)在绝热恒容的密闭容器中,进行反应:![]() ,该反应的平衡常数表达式为_______________________,对此反应下列说法正确的是_________。
,该反应的平衡常数表达式为_______________________,对此反应下列说法正确的是_________。
a.若混合气体密度保持不变,则已达平衡状态
b.从反应开始到平衡,容器内气体的压强保持不变
c.达平衡后若再充入一定量![]() ,平衡常数保持不变
,平衡常数保持不变
d.分离出![]() ,正、逆反应速率均保持不变
,正、逆反应速率均保持不变
(3)向![]() 恒温恒容密闭容器中通入
恒温恒容密闭容器中通入![]()
![]() 和
和![]()
![]() ,分别进行
,分别进行![]() 三组实验。在不同条件下发生反应:
三组实验。在不同条件下发生反应:![]() ,反应体系总压强随时间的变化曲线如图所示,则三组实验温度的大小关系是
,反应体系总压强随时间的变化曲线如图所示,则三组实验温度的大小关系是![]() ______
______![]() ______
______![]() (填“
(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”);实验
”);实验![]() 从反应开始至平衡时,反应速率
从反应开始至平衡时,反应速率![]() ______________。
______________。

II.![]() 溶液吸收法
溶液吸收法
常温下,用![]() 溶液吸收
溶液吸收![]() 的过程中,溶液
的过程中,溶液![]() 随吸收
随吸收![]() 物质的量的变化曲线如图所示。
物质的量的变化曲线如图所示。

(4)常温下,![]() 的二级电离平衡常数
的二级电离平衡常数![]() 的数值为_________________。
的数值为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是
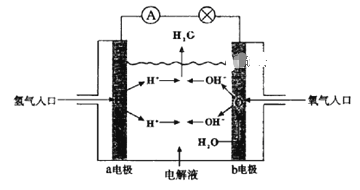
A. a电极是负极
B. 氢氧燃料电池是一种具有应用前景的绿色电源
C. b电极的电极反应为:4OH--4e-=2H2O+O2↑
D. 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入NaOH、Ca(OH)2、NaAlO2的混合溶液中,则生成沉淀的物质的量与通入CO2的体积的关系可表示为( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com