
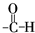
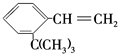
 滴入溴水后生成产物的结构简式为
滴入溴水后生成产物的结构简式为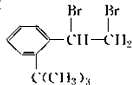 ,滴入酸性高锰酸钾溶液发生碳碳双键的氧化反应,生成物的结构简式为
,滴入酸性高锰酸钾溶液发生碳碳双键的氧化反应,生成物的结构简式为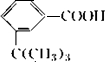 ,故答案为:
,故答案为: ;
;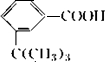 ;
;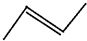 ,故答案为:
,故答案为: .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、K+、Cu2+、Na+、OH- |
| B、K+、H+、NO3-、CO32- |
| C、Ba2+、K+、Cl-、SO42- |
| D、K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
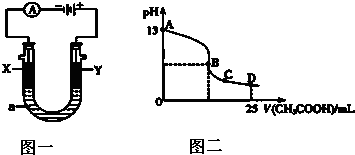
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
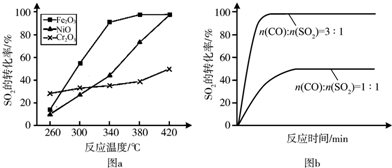
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
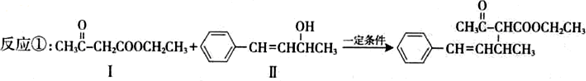
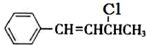 可生成化合物Ⅱ,所需的反应条件为
可生成化合物Ⅱ,所需的反应条件为查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑦ | ⑤ | ⑥ | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制取溴苯:将铁屑、溴水、苯混合加热 |
| B、实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 |
| C、鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 |
| D、检验卤代烃中的卤原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀的颜色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com