
| A. | 碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| B. | 用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O | |
| C. | NH4HSO4溶液与过量NaOH稀溶液反应:NH4++OH-=NH3•H2O | |
| D. | FeBr2溶液中通入少量Cl2:2Fe2++2Br-+Cl2=2Fe3++Br2+2Cl- |
分析 A.醋酸为弱酸,离子方程式中醋酸不能拆开;
B.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
C.氢氧化钠溶液过量,铵根离子和氢离子都参与反应;
D.氯气少量,亚铁离子优先反应,溴离子不反应.
解答 解:A.醋酸和碳酸钙都需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故A错误;
B.用烧碱溶液吸收氯气,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,故B正确;
C.NH4HSO4溶液与过量NaOH稀溶液反应生成硫酸钠、一水合氨和水,正确的离子方程式为:H++NH4++2OH-=NH3•H2O+H2O,故C错误;
D.FeBr2溶液中通入少量Cl2,由于还原性Fe2+>Br-,则氯气少量时亚铁离子优先反应,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故D错误;
故选B.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ag+、PO43-、Cl- | B. | Fe3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、H+ | D. | Al3+、Mg2+、SO42-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂在放电时做正极材料,充电时为阳极材料 | |
| B. | 电池在放电时,Li+向负极移动 | |
| C. | 该电池充电时阳极的反应为:LixV2O5-xe-=V2O5+xLi+ | |
| D. | V2O5只是锂发生反应的载体,不参与电池反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①③ | C. | ②④⑤⑥⑦ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、SCN-、CO32-、K+ | B. | SO32-、S2-、Al3+、Na+ | ||
| C. | NO3-、CH3COO-、Ba2+、Cl- | D. | SO42-、NH4+、ClO-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
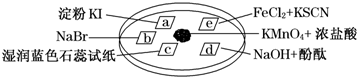
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝 | 氧化性:Cl2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变血红色 | 还原性:Fe2+>Cl- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解反应肯定是吸热反应 | |
| B. | 物质燃烧和中和反应均放出热量 | |
| C. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| D. | 化学反应是吸热还是放热决定于生成物和反应物具有的总能量大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备AlCl3晶体:将AlCl3溶液加热、蒸干,并灼烧 | |
| B. | 证明某卤代烃中的碘原子:在卤代烃中滴加NaOH溶液,振荡后滴加AgNO3溶液 | |
| C. | 鉴别乙醇、乙醛、乙酸三种物质的水溶液:用新制碱性氢氧化铜悬浊液 | |
| D. | 检验甲酸中混有甲醛:可先向样品中加入足量NaOH溶液中和甲酸,再进行银镜反应实验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com