
����Ŀ����A���ijЩ���ʼ��仯���ﳣ��������̫���ܵ�ء��뵼����ϵȡ�
(1)��̬ʱ��ԭ�Ӻ���ĵ����Ų�ʽΪ____________��
(2)����������ͬ����,����Ԫ�صĵ�һ�����ܴӴ�С˳��Ϊ____________(��Ԫ�ط��ű�ʾ)��
(3)��̬SeO3���ӵ�����ṹΪ____________,��SeO3��Ϊ�ȵ������һ������Ϊ____________(�ѧʽ)��
(4)��Ԫ�ؾ���ȱ������,����仯�����������мӺ��ԡ�
������(H3BO3)��һԪ����,д��������ˮ��Һ�еĵ��뷽��ʽ____________��
������(H3BO3)��һ�־���Ƭ��ṹ�İ�ɫ����,���ڵ�H3BO3���Ӽ�ͨ���������(��ͼ1)����1 mol H3BO3�ľ�������____________mol���,____________mol�Ҽ���H3BO3��B��ԭ���ӻ�����Ϊ____________��
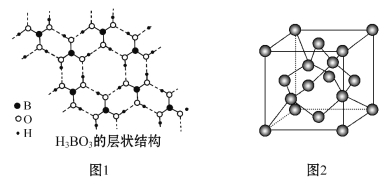
(5)���ij�ֵ��ʵľ�����ͼ2��ʾ�����ù辧����ܶ�Ϊ��g��cm-3,�����ӵ�����ֵΪNA,�����������������ԭ��֮��ľ���Ϊ________cm(�ô���ʽ��ʾ����)
���𰸡�(1)1s22s22p63s23p63d104s24p3(��[Ar]3d104s24p3)
(2)Br>As>Se
(3)ƽ�������� C![]() ��N
��N![]()
(4)��H3BO3+H2O![]() [B(OH)4]-+H+
[B(OH)4]-+H+
��3 6 sp2
(5)![]() ��
��![]()
��������(1)����33��Ԫ��,����ԭ�Ӻ�������Ų����ɿ���д�������Ų�ʽΪ1s22s22p63s23p63d104s24p3(��[Ar]3d104s24p3)��
(2)As��Se��Br����ͬһ������ԭ������������,������Ԫ���������ڵڢ�A�塢�ڢ�A�塢�ڢ�A��,�ڢ�A��Ԫ�ش���������Ԫ�صĵ�һ������,����3��Ԫ�صĵ�һ�����ܴӴ�С˳��ΪBr>As>Se��
(3)��̬SeO3����������ԭ�ӵļ۲���Ӷ���Ϊ![]() =3,�µ��Ӷ�,���Է��ӹ���Ϊƽ��������,����Ϊ�ȵ�����Ҫ��ԭ��������ͬ,�۵���������ͬ,������SeO3��Ϊ�ȵ������һ������ΪC
=3,�µ��Ӷ�,���Է��ӹ���Ϊƽ��������,����Ϊ�ȵ�����Ҫ��ԭ��������ͬ,�۵���������ͬ,������SeO3��Ϊ�ȵ������һ������ΪC![]() ��N
��N![]() ��
��
(4)������ΪһԪ����,��ˮ��Һ��������������,����뷽��ʽΪH3BO3+H2O![]() [B(OH)4]-+H+;
[B(OH)4]-+H+;
�ڸ���1������������γ�3�����,1������������γ�6���Ҽ�,��1 mol H3BO3�ľ�����������ʵ�����3 mol,�Ҽ���6 mol;
����ͼ֪,����(H3BO3)��ÿ����ԭ������3����ԭ���Ҳ����µ��Ӷ�,�ݴ�ȷ����ԭ���ӻ���ʽΪsp2��
(5)�þ�����Si����=8��![]() +6��
+6��![]() +4=8,�ʾ�������Ϊ
+4=8,�ʾ�������Ϊ![]() g=
g=![]() g,�辧����ܶ�Ϊ��g��cm-3,���ⳤ=
g,�辧����ܶ�Ϊ��g��cm-3,���ⳤ=![]() cm,����Խ��߳���Ϊ
cm,����Խ��߳���Ϊ![]() ��
��![]() cm,�������������ԭ��֮��ľ���Ϊ
cm,�������������ԭ��֮��ľ���Ϊ![]() ��
��![]() cm��
cm��![]() =
=![]() ��
��![]() cm��
cm��


 �ƸԹھ��ο���ϵ�д�
�ƸԹھ��ο���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɡ�
��ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼ1װ����һ�������ͬ����Ԫ��C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о���
��ͬѧ�������ͼ2װ������֤±��Ԫ�����ʵĵݱ���ɣ�ͼ2��A��B��C�����ֱ���մ��NaBr��Һ������ʪ��ĵ���KI��ֽ��ʪ��ĺ�ֽ��
��֪������Ũ�������������ܷ�Ӧ����������
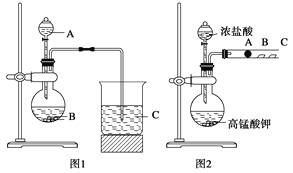
��1������������������ѡ����ͬѧ��Ƶ�ʵ�����õ����ʣ�ͼ1���Լ�A��BΪ������ţ�____��
��ϡ������Һ�� ��Ũ��� ��̼���Ʒ�ĩ����Na2SO3��Һ
д��ͼ1��ƿ�з�����Ӧ�����ӷ���ʽΪ__________________________________________��
��2����ͬѧ����ʵ��ͼ1�ձ�������Ϊ____________________________________��
��3����ͬѧ����ʵ��ͼ2��B��������Ϊ__________________________________��
��4��д��ͼ2��A��������Ӧ�����ӷ���ʽΪ__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�����������+3�����Ļ�������ǣ� ��
�����ۺ�ϡ����ڹ�������ϡ����۹�������FeCl3����ˮ��FeCl2��FeO��ϡ��������ۺ�����ϡ���� ����ƬͶ��CuSO4��Һ������Cl2��ȼ�գ�
A.�ڢۢܢ�
B.�ܢݢޢ�
C.�ۢܢޢ�
D.�ڢۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯������������Ӧ����
A��Cl2��2e����2Cl�� B��S2��-2e����S
C��Ag����e��=Ag D��Cr2O72����14H����6e��=2Cr3+��7H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Һ���ܴ���������ǣ�������
A.Fe3+��NH4+��SCN����Cl��
B.Na+��Mg2+��NO3����SO42��
C.Al3+��Fe2+��NO3����Cl��
D.K+��Na+��Cl����SiO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����ʽΪC8H14N2O3�Ķ��ģ���ˮ���õ�������CH3CH��NH2��COOH����һ�ְ�����R����R�ķ���ʽΪ��������
A.C5H9NO
B.C5H9NO2
C.C5H9NO3
D.C5H9NO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��D��E��F����Ԫ�ص�ԭ��������������FΪ����Ԫ���⣬�������־��Ƕ�����Ԫ�ء���֪����F�ĵ���Ϊ����������Ľ���֮һ��ԭ���������2�����ӣ���Eԭ�ӵļ۵����Ų�Ϊmsnmpn��Bԭ�ӵĺ���L�������Ϊ��������A��Dԭ��p����ĵ������ֱ�Ϊ2��4����ش��������⣺
(1)F���ȶ���̬���ӵĵ����Ų�ʽ��________________��A��B��D��E����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ________________(��Ԫ�ط��ű�ʾ)��
(2)����B�ļ��⻯�������ԭ�ӵĹ���ӻ�������________�����ӵ����幹��Ϊ________________�����⻯��������D�ļ��⻯�����Ҫԭ����______________��
(3)Dԭ�ӷֱ���A��Bԭ���γɵĵ����У����ļ��Խ�ǿ����________(�þ���Ļ�ѧ����ʾ)��
(4)��ͼ��ʾ�ľ�������A��D��Ԫ����ɵģ������йظþ����˵������ȷ����________��
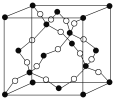
a���þ���Ļ�ѧʽΪAD
b���þ�����A��Dԭ�Ӽ��γɵ���˫��
c���þ����۵���ܱ�SiO2�����
d���þ��������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������·ǹ�̬�������ǣ� ��
A.��֬�ᣨC15H31COOH��
B.���ᣨC17H33COOH��
C.���ᣨHOOC��COOH��
D.�����ᣨH2N��CH2COOH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E��F��G����Ԫ�������ǵ�ԭ��������������A������Ԫ����ԭ�Ӱ뾶��С��Bԭ�Ӻ��������6�ֲ�ͬ�˶�״̬��D��C��E�����ڣ�A��D��E����Ԫ�ص�ԭ������֮��Ϊ25��E2����F������ͬ�ĺ�������Ų���G����������25����ش��������⣺
(1)д��Ԫ��G�Ļ�̬ԭ����Χ�����Ų�ʽ________��B��C��D����Ԫ�طֱ��γɵ�����⻯��ķе���ߵ���________(�û�ѧʽ��ʾ)��
(2)������Ԫ���е�����Ԫ����ɵ�һ����������D��һ��ͬ����������ӻ�Ϊ�ȵ��������������ӻ�ѧʽΪ________��
(3)������Ԫ����ɵ����ڷǼ��Է�����VSEPRΪֱ���ε����ĵ���ʽ________(��дһ��)��
(4)M����4��Cԭ����ɵ�һ�ֲ��ȶ��Ķ�ԭ�ӵ��ʷ�����M������Cԭ���ӻ���ʽΪsp3�ӻ���M���ӵ����幹��Ϊ________��
(5)ijһ���Ե�صı������Ϳɴ���ʱ�������ͨ�ɵ�������������ڴ�����������ŵ��������õ�ص�����������Ʒ֮һ�����ĸ���������Zn������������G��һ�ֳ������������������KOH���õ�ص�������ӦʽΪ______________��
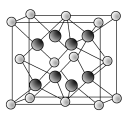
(6)������Ԫ���е縺������Ԫ�غ͵�һ��������С��Ԫ���γɵ�ij������N�ľ�������ͼ��ʾ��������N������������������ܽ�С����______(�ѧʽ)����֪�û�����ľ����߳�Ϊa pm����û�������ܶ�Ϊ________g��cm��3(ֻҪ���г���ʽ�����ؼ������ֵ�������ӵ���������ֵΪNA��1 pm��10��10cm)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com