
【题目】为证明溴乙烷中溴元素的存在,现有以下操作:①加入硝酸银溶液②加入氢氧化钠溶液③加热④加入蒸馏水⑤加入稀硝酸至溶液呈酸性⑥加入氢氧化钠的醇溶液,下列是按一定顺序进行的操作步骤,其中正确的是( )
A. ④③①⑤ B. ④③⑤① C. ④⑥③① D. ②③⑤①
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】乙二胺(H2NCH2CH2NH2 )是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是

A. 常温下,pKb2=-1gKb2 =7.15
B. 溶液中水的电离程度:a点大于b点
C. H3NCH2CH2NH2Cl2 溶液中c(H+)>c(OH-)
D. 曲线G代表pH 与![]() 的变化关系
的变化关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某化学兴越小组对其组成进行探究。
已知Cu2O在酸性溶液中会发生歧化反应:Cu2O+2H+=Cu+Cu2++H2O。
方案一:
(1)学生甲取少量样品于烧杯中,加入过量浓硝酸,产生一种红棕色的气体。由此可得出样品中一定含有_______,写出产生上述气体的化学方程式_____________。
(2)进一步探究样品中另一种成分。实验操作步骤为:取少量上述反应后溶液,加入______(填化学式)溶液,观察现象。
方案二:
(3)学生乙取少量样品于烧杯中,加入过量稀硫酸,并作出如下假设和判断,结论正确的____。
A.若固体全部溶解,说明样品一定含有Fe2O3,一定不含有Cu2O
B.若固体部分溶解,说明样品一定含有Cu2O,一定不含有Fe2O3
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,说明样品一定含有Fe2O3和Cu2O
方案三:
学生丙利用下图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:
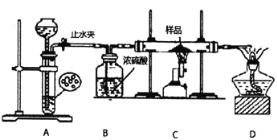
(4)装置A是氢气的发生装置,可以使用的药品是______(填选项)。
A.氢氧化钠溶液和铝片 B.稀硝酸和铁片 C.稀硫酸利锌片 D.浓硫酸和镁片
(5)下列实验步骤的先后顺序是_____(填序号)。
①打开止水夹 ②关闭止水夹 ③点燃C处的酒精喷灯
④熄灭C处的酒精喷灯 ⑤收集氢气并验纯
(6)假设样品全部参加反应生成相应金属单质,若实验前样品的质量为15.2g,实验后称得装置C中固体的质最为12.0g。则样品的组成是(若有多种成分,则须求出各成分的质量)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境已成为当前和未来的全球性的重大课题之一,下列因为人类生产对环境破坏而带来的后果是( )
①土地沙漠化 ②酸雨 ③水资源危机 ④南极上抽样空洞 ⑤沙尘暴.
A.①②⑤
B.①②④⑤
C.②⑤
D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭属于不可再生资源,高效、清洁地利用煤炭资源至关重要。请回答下列问题:
(1)煤的干馏。煤的干馏反应中△S_____0(填“>”“<”或“=”)。
(2)煤的液化。原理是C(s)+H2O(g)![]() CO(g)+H2(g) △H= akJ/mol;CO(g)+2H2(g)
CO(g)+H2(g) △H= akJ/mol;CO(g)+2H2(g)![]() CH3OH(l) △H=bkJ/mol。则反应C(s)+ H2O(g)+H2(g)
CH3OH(l) △H=bkJ/mol。则反应C(s)+ H2O(g)+H2(g)![]() CH3OH(l) 的△H=______kJ/mol。
CH3OH(l) 的△H=______kJ/mol。
(3)煤的气化。原理是C(s) +2H2(g)![]() CH4(g) △H。在1L密闭容器中投入1mol碳,并充入2 mol H2,测得相关数据如图所示。
CH4(g) △H。在1L密闭容器中投入1mol碳,并充入2 mol H2,测得相关数据如图所示。

①有关图1、图2 的说法正确的有______(填标号)。
a.氢气的反应速率v(Z) >v(X) >v(Y)
b.T1<1000K
c.平衡常数K(X)=K(Y) >K(Z)
d.工业生产中,当温度为T2 时,压强越高,经济效益越好
②图2 中A 点对应的平衡常数Kp=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)煤生产水煤气和半水煤气。
①工业上用煤生产作为合成氨原料气的水煤气,要求气体中(CO + H2) 与N2的体积之比为3.1-3.2,发生的反应有C(s)+H2O(g)![]() CO(g) +H2(g).C(s) +1/2O2(g)
CO(g) +H2(g).C(s) +1/2O2(g)![]() CO(g)。从能量角度考虑,通入空气的目的是__________。
CO(g)。从能量角度考虑,通入空气的目的是__________。
②如图3是反应CO(g) +H2O(g) ![]() H2(g)+ CO2(g) △H<0 中CO 和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是_______(写出1种即可)。若t4 时刻通过改变容积的方法将压强增大为原来的2 倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。________
H2(g)+ CO2(g) △H<0 中CO 和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是_______(写出1种即可)。若t4 时刻通过改变容积的方法将压强增大为原来的2 倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾长石(K2Al2Si6O16)通常也称正长石,主要用于生产玻璃、陶瓷制品,还可用于制取钾肥。某学习小组以钾长石为主要原料,从中提取氧化铝、碳酸钾等物质,工艺流程如下:
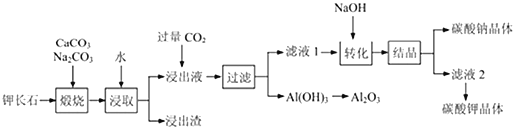
回答以下问题:
(1)请以氧化物组成的形式表示钾长石的化学式为_____________
(2)煅烧过程后,钾长石中的硅元素以______________(填化学式)的形式存在于浸出渣中;已知钾元素和铝元素在Na2CO3作用下转化为可溶性的KAlO2和NaAlO2,写出Al2O3与Na2CO3反应生成NaAlO2 的化学方程式______________________________。
(3)“浸取”过程中,需要将钾长石由块状固体粉碎为较小颗粒,其目的是___________
(4)“转化”时加入NaOH溶液的作用是_________________________ (用离子方程式表示)
(5)此工艺中可以循环利用的主要物质是___________、___________和水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.石油裂化的目的是获得更多的乙烯,丙烯等原料
B.石油分馏,煤的干馏发生的都是物理变化
C.油脂的皂化发生的是化学变化
D.向蛋白质溶液中分别加入硫酸铜,硫酸铵的浓溶液都可以发生盐析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com