
 生成铝的产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.请回答下列问题:
生成铝的产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.请回答下列问题:
| ||


科目:高中化学 来源: 题型:
| 资料卡片 | ||
| 物质 | 熔点/℃ | 沸点/℃ |
| SiCl4 | -70 | 57.6 |
| TiCl4 | -25 | 136.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
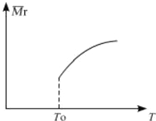 用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)
用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)| △ |
| 温度T | T1 | T2 | T3 |
| 平衡常数K | 1.2 | 2.5 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、②③⑤ |
| C、①④⑤ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 金属 状态 | c(H2SO4) /mol?L-1 | 溶液温度/℃ | 金属消失 的时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 丝 | 0.7 | 20 | 36 | 250 |
| 2 | 丝 | 0.8 | 20 | 35 | 200 |
| 3 | 粉末 | 0.8 | 20 | 35 | 25 |
| 4 | 丝 | 1.0 | ? | 35 | 125 |
| 5 | 丝 | 1.0 | 35 | 50 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它们都能与金属钠反应放出氢气,说明它们都是电解质 |
| B、它们都能发生酯化反应,反应中的断键位置也相同 |
| C、除去乙醇中的乙酸可加生石灰后再蒸馏 |
| D、用酸性K2Cr2O7检验司机是否酒后驾车,是利用了乙醇的氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com