
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为
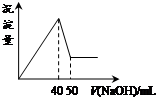
| A.1:3 | B.1:2 | C.1:1 | D.2:1 |
C
解析试题分析:首先发生反应Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,然后发生反应Al(OH)3+OH-═AlO2-+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为10mL,根据离子方程式Al3++3OH-═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的体积为10mL×3=30mL,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液40mL,计算沉淀Mg2+消耗的氢氧化钠溶液的体积为40mL-30mL=10mL,则n(Mg2+):n(Al3+)=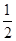 ×10mL:
×10mL: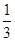 ×30mL=1:2,故原来混合溶液中Al2(SO4)3和MgSO4的物质的量浓度之比为1:1,故选C。
×30mL=1:2,故原来混合溶液中Al2(SO4)3和MgSO4的物质的量浓度之比为1:1,故选C。
考点:考查镁铝化合物性质、混合物的有关计算。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:单选题
取Na2O、Na2O2、Na2CO3的固体混合物做了以下实验,以下记录不符合事实的是
| A.加入水中,产生无色气体 |
| B.加入酚酞溶液中,溶液先变红后褪色 |
| C.在干空气中加热到400℃,质量减少 |
| D.与SO2反应后,检测到有Na2SO4生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
等体积、等物质的量浓度的稀硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为2:3,则甲、乙两烧杯中的反应情况可能分别是
| A.甲中酸过量,乙中碱过量 | B.甲中铝过量,乙中碱过量 |
| C.甲中酸过量,乙中铝过量 | D.甲、乙中都是铝过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将铁粉放入由盐酸、MgCl2溶液、FeCl3溶液、CuCl2溶液组成的混合液中,充分反应后,铁粉有剩余,则反应后的溶液中含有的大量阳离子是
| A.Cu2+ 和Fe2+ | B.H+ 和Cu2+ | C.Fe3+ 和Fe2+ | D.Fe2+ 和Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于Na2CO3和NaHCO3的性质比较中,不正确的是
| A.热稳定性: Na2CO3 > NaHCO3 |
| B.常温时在水中的溶解度:Na2CO3 > NaHCO3 |
| C.与稀盐酸反应的剧烈程度:Na2CO3 > NaHCO3 |
| D.等质量的固体与足量的盐酸反应放出CO2的质量:NaHCO3 > Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应并不改变的是
| A.Al和氢氧化钠溶液 | B.NaOH和CO2 |
| C.Na和O2 | D.AlCl3和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42- 的物质的量浓度为6 mol·L-1,则此溶液最多溶解铁粉的质量为( )
| A.5.6 g | B.11.2 g | C.22.4 g | D.33.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入到过量NaHCO3溶液中
④Na2O2投入FeCl2溶液中
| A.只有①④ | B.只有③ | C.只有②③ | D.只有①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com