
����Ŀ��Na2S2O3��5H2O����Ϊ��Ч���ȼ�����ҵ����������(FeS2)Ϊԭ���Ʊ������ʵ�������ͼ��
![]()
��֪��a.����A����ʹƷ����Һ��ɫ��������(H2S)����ܻ�õ�����
b.pHԼΪ11�������£����������������ο��Թ���������������Ρ�
�ش��������⣺
��1���������е�ԭ��B����ѡ��__(����ĸ���)��
A.NaCl��Һ B.Na2CO3��Һ C.Na2SO4��Һ
��2��ijС��ͬѧ����ͼװ��ģ���Ʊ�Na2S2O3�Ĺ���(����װ������ȥ)��

��A��ʹ��70�����������98%��Ũ���ᷴӦ���ʿ죬��ԭ����__��װ��B��������__��
��C���Ʊ�Na2S2O3������������Ӧ�У�Na2S+H2O+SO2=Na2SO3+H2S��__��Na2SO3+S![]() Na2S2O3��
Na2S2O3��
��3������ʦ����˴��������õ�����Ĺ��գ���������������ù�����ϡ�����ȡ���õ���������������壬�÷�Ӧ�Ļ�ѧ����ʽΪ__��
���𰸡�B �÷�Ӧ��ʵ����H+��SO32-��Ӧ��70%�������к�ˮ�϶࣬c(H+)��c(SO32-)���ϴ�����SO2���ʸ��죨����ǿ��Ũ�����������Է�����ʽ���ڣ� ��ֹ���� 2H2S+SO2=3S+2H2O(��2H2S+H2SO3=3S��+3H2O) FeS2+2HCl=FeCl2+H2S��+S��
��������
�������ڷ���¯��ȼ�������������������������A�Ƕ���������ҺD����Ũ������ȴ�ᾧ�õ���������ƾ��壬DΪNa2S2O3�����������������ο��Թ���������������Σ�����ҺCΪNa2SO3����������BҪ������SO2����Na2SO3������ԭ��B����Ϊ̼������Һ������������Һ���������Ϸ������
(1)B���ն�������ת��Ϊ�������ƣ�̼���ƿ������������Ӧ�����������ƣ���NaCl�� Na2SO4���������Ӧ��
��ѡB��
(2)��AΪ�Ʊ��������÷�Ӧ��ʵ����H+��SO32-��Ӧ��70%�������к�ˮ�϶࣬c(H+)��c(SO32-)���ϴ�����SO2���ʸ��죬��Ũ�����������Է�����ʽ���ڣ��������������Ũ�Ⱥܵͣ���˷�Ӧ��������������C����������Һ��Ӧ�õ����⣬�������������Ӧ�õ�S���ʣ�S�������������Ʒ�Ӧ�õ���������ƣ�C�з�Ӧ����װ����ѹǿ��С��Bװ�õ������Ƿ�ֹ������
��Ϊ���÷�Ӧ��ʵ����H+��SO32-��Ӧ��70%�������к�ˮ�϶࣬c(H+)��c(SO32-)���ϴ�����SO2���ʸ��죨����ǿ��Ũ�����������Է�����ʽ���ڣ�����ֹ������
��C���Ʊ�Na2S2O3������������Ӧ�У�Na2S+H2O+SO2=Na2SO3+H2S��2H2S+SO2=3S+2H2O(��2H2S+H2SO3=3S��+3H2O) ��Na2SO3+S![]() Na2S2O3��
Na2S2O3��
����2H2S+SO2=3S+2H2O(��2H2S+H2SO3=3S��+3H2O)��
(3)��������Ϣ��֪��FeS2��HCl��Ӧ����H2S��S��ͬʱ������FeCl2��������Ϣд����Ӧ����ʽΪ��FeS2+2HCl=FeCl2+H2S��+S����
����FeS2+2HCl=FeCl2+H2S��+S�� ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�����������õ�������ѧ���ʣ����㷺Ӧ�������������С��Ӻ��ܷ���(��CoO��Co2O3������Al��Li��)����ȡ��CoCl2��6H2O������������ʾ��
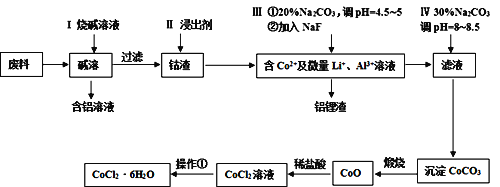
��ش��������⣺
(1)����I����Ҫ�����Ļ�ѧ��Ӧ����ʽΪ______��
(2)��֪Co2O3����ǿ�����ԣ�������II�н�����Ϊ���ᣬ��ɵĺ����_______��
(3)�������Тٵ�Ŀ���dz�ȥAl3+��д���ò���Ӧ�����ӷ���ʽ______��
(4)����ʵ��������CoCO3������Ĺ��������������ƾ��ƺͲ������⣬����______��______(����������)��
(5)����������HCl��Χ�н��еģ��䲽����______��_____�����ˡ�ϴ�ӡ����ϴ�ӹ����п����ù�ҵ�ƾ�����ˮ�����ŵ���_____��
(6)ijͬѧ�ñ���������Һ�ζ�δ֪Ũ�ȵ�CoCl2��Һ�����п���Ϊָʾ������____(��ѡ������������ӵ���ɫ����)
A��KCl B��KSCN C��K2CrO4 D��K2S
��֪����������20��ʱ����ɫ��Kspֵ���±�
��ѧʽ | AgCl | AgSCN | Ag2S | Ag2CrO4 |
��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ |
Ksp | 2.0��10-10 | 1.0��10-12 | 2.0��10-48 | 2.0��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1799����Ӣ����ѧ�Һ���������ά����һ����������N2O��������������������ã����Ҷ����ࡢ�ε��������˺����㷺Ӧ����ҽѧ�����С�
��1��һ�����������ڱ���������������������������������ڴ����·ֽ��Ƶã��÷�Ӧ�Ļ�ѧ����ʽΪ ___��
��2����֪��Ӧ2N2O(g)=2N2(g)+O2(g)����H=�C163kJ��mol��1��1molN2(g)��1molO2(g)�����л�ѧ������ʱ�ֱ���Ҫ����945kJ��498kJ����������1molN2O(g)�����л�ѧ������ʱ��Ҫ���յ�����Ϊ______kJ��
�ڵ�һ�ܶ�����Ϊ���µĺ��������У���Ӧ2N2O(g)=2N2(g)+O2(g)�IJ���ʵ���������£�
![]()
����0��20minʱ�Σ���Ӧ����v(N2O)Ϊ ___mol��L-1��min-1��
����N2O��ʼŨ��c0Ϊ0.150mol/L ����Ӧ��30minʱN2O��ת������=___��
�۲�ͬ�¶ȣ�T���£�N2O�ֽ��˥������ʼѹǿ�ı仯��ϵ��ͼ��ʾ��ͼ�а�˥��ָ��һŨ��N2O����һ��ʱ�������Ӧʱ�䣩����T1 ___T2������>������=������<���������¶�ΪT1����ʼѹǿΪp0����Ӧ��t1minʱ����ϵѹǿp= ___����p0��ʾ����

��4�������������ܴ�������N2O�ķֽ����ʣ���Ӧ����Ϊ��
��һ�� I2(g) = 2I(g) ���췴Ӧ��
�ڶ��� I(g)+N2O(g)��N2(g)+IO(g) ������Ӧ��
������ IO(g)+N2O(g)��N2(g)+O2(g)+I(g) ���췴Ӧ��
ʵ�����������ʱNO�ֽ����ʷ���v=k��c(N2O)��[c(I2)]0.5��kΪ���ʳ����������б�����ȷ����___������)��
A���¶����ߣ�kֵ���� B����һ�����ܷ�Ӧ�������������
C���ڶ�����ܱȵ������� D��I2Ũ����N2O�ֽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F���ֶ���������Ԫ�أ�ԭ������������������B�ĵ����ڳ�����Ϊ˫ԭ�ӷ��ӣ�����A�ĵ��ʿ��γ���̬����X��X��ˮ��Һ�ʼ��ԣ�D�ļ���������X������ͬ����������D��ͬ����Ԫ����ԭ�Ӱ뾶����Ԫ�أ�EԪ�ص�ԭ�������ȴ�������������ӣ�C��F����Ԫ�ص�ԭ������㹲��13�����ӡ���
��1��X�Ļ�ѧ����Ϊ__________��
��2��B���ʵĽṹʽΪ__________��E����̬�⻯��ĵ���ʽΪ__________��C��D�γɵ����ֻ������У�����һ�����ʺ����������͵Ļ�ѧ�����ֱ�Ϊ______________������������______________(�������ӻ��������������ۻ�������)��
��3��B��C��E�ֱ���A�γɵĻ����������ȶ�����__________(д��ѧʽ)��
��4��D��ͬ���ڼ������������Ӱ뾶��__________(������������С��)��Ԫ�ء�
��5��F�ĵ����ڷ�Ӧ�г���________��(����������������ԭ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɵ���߷��Ӳ���PPV�ķ�Ӧ���¡�����˵����ȷ���ǣ� ��
 +��2n-1��HI
+��2n-1��HI
A. �ϳ�PPV�ķ�ӦΪ�Ӿ۷�Ӧ
B. 1molPPV�������4 molH2�����ӳɷ�Ӧ
C.  ����ˮ�ӳɺ�IJ��������14��ԭ�ӹ�ƽ��
����ˮ�ӳɺ�IJ��������14��ԭ�ӹ�ƽ��
D.  �ͱ���ϩ��Ϊͬϵ��
�ͱ���ϩ��Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������̬����ɵĻ���ȡ��2.24L����״���£����ȼ�գ��õ�0.16mol������̼�����3.6gҺ̬ˮ���ݴ��ж����з����в���ȷ����
A. �˻�������п��ܺ�������
B. ��������һ�����м���
C. �˻��������һ�������б���
D. ������������ϩ�����Ļ�����壬���������ϩ�������Ϊ2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����˾ƥ����һ�ֽⶾ��ʹҩ����A��һ���л�����ԭ�ϣ���ͼ������Ϊ��ʼԭ����ƺϳɰ�˾ƥ�ֹ�ϵͼ��

��֪���������������ױ�������
�ش��������⣺
��1��C�Ľṹ��ʽΪ___________��
��2����Ӧ�ݵķ�Ӧ����___________���ڢ�֮ǰ��Ƣ���һ����Ŀ����___________��
��3��F �к��������ŵ�����________��
��4��G����˾ƥ�֣�������NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ______________��
��5���������������� E ��ͬ���칹����________�֡�д���˴Ź���������������壬�����֮��Ϊ 1��2��2��2��1 �Ľṹ��ʽ��_______��ֻдһ�֣���
a������OH b���ܷ���ˮ�ⷴӦ c���ܷ���������Ӧ
��6�����üױ�Ϊԭ�ϣ�������Ϻϳ�·�ߺ�����������Ϣ�ϳ���ͼ��ʾ�Ĺ��ܸ߷��Ӳ��ϣ����Լ���ѡ����________

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ����ѡ��3�����ʽṹ�����ʣ�
2016��ŵ������ѧ�������������ӻ�����ƺͺϳ���������ͻ���ɾ͵���λ��ѧ�ң����о�����֮һ�����ӿ����������������ӱ�����������ӻ����������йء��ش��������⣺
��1�����嶡����[4]����(��ͼ����ʾ)��������B��Ԫ�ض�Ӧ���ӵ���ȡ����La3����Sc2����д����̬����������(Sc2��)�ĺ�������Ų�ʽ��________�����е���ռ�ݵĹ����Ϊ________����
��2�����嶡����[4]������4���ǻ����ɱ��ף������ǻ���ԭ�ӵ��ӻ���ʽΪ________���ǻ�����������Ϊ________��
��3����ͬ��С�ı�������ʶ��ijЩ���ӣ��磺![]() ��SCN���ȡ�һ�������£�SCN����MnO2��Ӧ�ɵõ�(SCN)2����д��(SCN)2�Ľṹʽ______________________________��
��SCN���ȡ�һ�������£�SCN����MnO2��Ӧ�ɵõ�(SCN)2����д��(SCN)2�Ľṹʽ______________________________��
��4��NH3�����ڶ�������ʱH��N��H����Ϊ106.7������ͼ [Zn(NH3)6]2�����ӵIJ��ֽṹ�Լ�H��N��H���ǵIJ���ֵ�������������H��N��H���DZ�Ϊ109.5����ԭ��______��
��5���Ⱥ�ɫ�İ��ʻ�����[Co2(CO)8]���۵�Ϊ52�����������Ҵ������ѡ������л��ܼ����þ�������________���壬���ʻ�������Һ���б������ƻ�ԭ�����ʻ�������[NaCo(CO)4]�����Ȼ��������к��еĻ�ѧ��Ϊ_________________��
��6����֪C60���ӽṹ��C60����ʾ��ͼ(��ͼ����ͼ����ʾ)��

��һ��C60�����к��������ĸ���Ϊ________��C60�����ܶȵļ���ʽΪ________ g��cm��3��(NAΪ����٤��������ֵ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯������;�dz��㷺���ش��������⣺
��1�����ķ���ϩ��Ʒ����Ϊ���ط�������������ճ��Ϳ�㡣����һ�����壬�þ�����һ����ƽ�����������ϸ�����λ����Ķ��ؾ��塣��ͨ��____�������־��塢����ͷǾ��塣
��2����̬�ࣨSb��ԭ�Ӽ۵����Ų��Ĺ��ʽΪ____��[H2F]+[SbF6]���������ࣩ��һ�ֳ�ǿ�ᣬ����[H2F]+�������ӵĿռ乹��Ϊ______������д��һ����[H2F]+������ͬ�ռ乹�ͺͼ�����ʽ�ķ��Ӻ������ӷֱ���_______��_________��
��3�����ᣨH3BO3�����ķ�����泥�NH4BF4����������Ҫ�Ļ�����;��
��H3BO3��NH4BF4�漰������Ԫ���еڶ�����Ԫ�صĵ�һ�������ɴ�С��˳��_____����Ԫ�ط��ţ���
��H3BO3�������ܵ����H+����ˮ�����һ��OH������[B(OH)4]���������������ԡ�[B(OH)4]����Bԭ�ӵ��ӻ�����Ϊ_____��
��NH4BF4���ķ�����泥�����������ͭ�������ۼ����ܸ�ʴ�����ȡ��ķ�������д���_______������ţ���
A ���Ӽ� B ���� C ���� D ��� E ���»���
��4��SF6���㷺������ѹ�����豸��Ե���ʡ�SF6��һ�ֹ��ۻ������ͨ��������Born-Haberѭ��������������ͼ����ͼa����������ϵ�ļ��ܡ���S��F�ļ���Ϊ_______kJ��mol-1��

��5��CuCl���۵�Ϊ426�棬�ۻ�ʱ���������磻CuF���۵�Ϊ908�棬�ܶ�Ϊ7.1g��cm-3��
��CuF��CuCl�۵�ߵ�ԭ����_____________��
�� ��֪NAΪ�����ӵ�������CuF�ľ����ṹ������ͼb������CuF�ľ�������a=__________nm ���г�����ʽ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com