
����Ŀ����Ԫ�����������õ�������ѧ���ʣ����㷺Ӧ�������������С��Ӻ��ܷ���(��CoO��Co2O3������Al��Li��)����ȡ��CoCl2��6H2O������������ʾ��
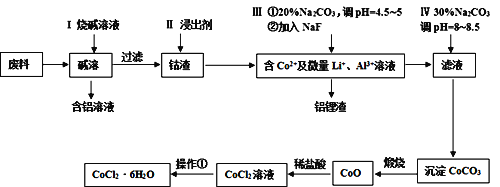
��ش��������⣺
(1)����I����Ҫ�����Ļ�ѧ��Ӧ����ʽΪ______��
(2)��֪Co2O3����ǿ�����ԣ�������II�н�����Ϊ���ᣬ��ɵĺ����_______��
(3)�������Тٵ�Ŀ���dz�ȥAl3+��д���ò���Ӧ�����ӷ���ʽ______��
(4)����ʵ��������CoCO3������Ĺ��������������ƾ��ƺͲ������⣬����______��______(����������)��
(5)����������HCl��Χ�н��еģ��䲽����______��_____�����ˡ�ϴ�ӡ����ϴ�ӹ����п����ù�ҵ�ƾ�����ˮ�����ŵ���_____��
(6)ijͬѧ�ñ���������Һ�ζ�δ֪Ũ�ȵ�CoCl2��Һ�����п���Ϊָʾ������____(��ѡ������������ӵ���ɫ����)
A��KCl B��KSCN C��K2CrO4 D��K2S
��֪����������20��ʱ����ɫ��Kspֵ���±�
��ѧʽ | AgCl | AgSCN | Ag2S | Ag2CrO4 |
��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ |
Ksp | 2.0��10-10 | 1.0��10-12 | 2.0��10-48 | 2.0��10-12 |
���𰸡�2Al + 2NaOH +2H2O=2NaAlO2 + 3H2����2Li + 2H2O=2 Li OH + H2�� ������ж��������� 2Al3+ + 3CO32- + 3H2O=2Al(OH)3�� + 3CO2�� ���� ������ ����Ũ�� ��ȴ�ᾧ ���پ�����ܽ���ʧ C
��������
���ܷ���(��CoO��Co2O3������Al��Li)�����Һ��Al������ǿ����Һ����ƫ�����κ���������ܹ���ˮ�ܽ⣬���˵õ������ͺ�����Һ�������м���������õ�����Co2+����Li+��Al3+��Һ�������Һ�м���20%̼������Һ������Һ��pHΪ4.5-5֮�䣬Ȼ�����NaF�����˵õ����������Һ����Һ�м���30%̼������Һ������Һ��pHΪ8-8.5���õ�CoCO3����������̼���ܵõ�CoO��CoO�����ᷴӦ����CoCl2������Ũ������ȴ�ᾧ�����˷����CoCl2��6H2O�ᾧˮ����ݴ˷������
(1)����I��Al������ǿ����Һ����ƫ�����κ���������ܹ���ˮ�ܽ⣬��������Ҫ��ѧ��Ӧ����ʽ��2Al + 2NaOH +2H2O=2NaAlO2 + 3H2����2Li + 2H2O=2 Li OH + H2�����ʴ�Ϊ��2Al + 2NaOH +2H2O=2NaAlO2 + 3H2����2Li + 2H2O=2 Li OH + H2����
(2)Co2O3����ǿ�����ԣ�������II�н�����Ϊ���ᣬ�����е���Ԫ�ؿ��ܱ�����������������Ⱦ�������ʴ�Ϊ��������ж���������(��������������Ⱦ����)��
(3)�������Тٵ�Ŀ���dz�ȥAl3+��������̼�����ܹ�����˫ˮ�ⷴӦ����Ӧ�����ӷ���ʽΪ2Al3+ + 3CO32- + 3H2O=2Al(OH)3�� + 3CO2�����ʴ�Ϊ��2Al3+ + 3CO32- + 3H2O=2Al(OH)3�� + 3CO2����
(4)ʵ��������CoCO3��Ҫ�������н��У�����Ĺ��������������ƾ��ƺͲ������⣬���������������ǣ��ʴ�Ϊ�������������ǣ�
(5)CoCl2�ܹ�ˮ�⣬���ɵ��Ȼ������ӷ�����˲���������Ҫ��HCl��Χ�н��У���CoCl2��Һ�л��CoCl2��6H2O���壬��Ҫ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����ϴ�ӹ����п����ù�ҵ�ƾ�����ˮ�����پ�����ܽ���ʧ���Ҿƾ��������ӷ������ھ������ʴ�Ϊ������Ũ������ȴ�ᾧ�����پ�����ܽ���ʧ��
(6)ijͬѧ�ñ���������Һ�ζ�δ֪Ũ�ȵ�CoCl2��Һ�����ݼ���������20��ʱ����ɫ��Kspֵ���ζ���������Ҫ�����Ե�����Ӧ��ѡ��K2CrO4Ϊָʾ�����ʴ�Ϊ��C��


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڹʹ�������ⲿ��¼Ƭ����ڹŴ���ͭ������������ij��ѧС�����Ȥ����������������ﱣ������ּ��
��1�����ĸ��н̲ĵ�֪ͭ��ΪCu2(OH)2CO3���׳�ͭ�̣��������ᡣͭ����һ���̶��Ͽ���������ͭ����������ֵ�������γ�ͭ�̵�������Cu��_______��
��2�����������й�֪�����˽ͭ��ijɷַdz����ӣ���Ҫ�ɷ���Cu2(OH)2CO3��Cu2(OH)3Cl������ѧ�ҽ�ͭ���Ϊ������к��⣬�ṹ��ͼ��ʾ��
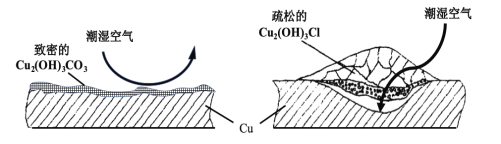
Cu2(OH)2CO3��Cu2(OH)3Cl�ֱ�����������к��⣬�����ԭ��_____________��
��3��������ʾ�к�����γɹ����л����CuCl����ɫ������ˮ�Ĺ��壩��������ͼ�ش�
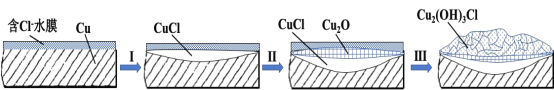
�� ���̢��������Ӧ����___________��
�� ���̢��ĵ缫��Ӧʽ��_____________��
��4����ͭ���������������ַ�����
�������������������ʴ����ֱ�ӷ���2%-3%����������Һ�н��ݳ��⣻
����̼���Ʒ�������ʴ�������ں�Na2CO3�Ļ�����Һ�н��ݣ�ʹCuClת��Ϊ���ܵ�Cu2(OH)2CO3��
����BTA��������
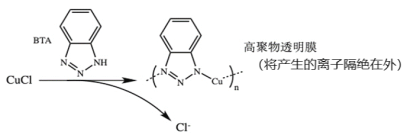
��ش��������⣺
��д��̼���Ʒ������ӷ���ʽ___________________��
�����ַ����У�BTA������Ӧ����Ϊ�ձ飬��������ܵ��ŵ���___________��
A������ͭ�������γ�һ�����ܵ�������Ĥ
B���滻������е�Cl-���ܹ���Ч�ij�ȥ�к���
C�����������ȣ����ƻ����⣬���Ա�����ͭ����������ֵ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2 L�ܱ������ڣ�800 ��ʱ��Ӧ��2NO��g����O2��g�� ![]() 2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
n��NO����mol�� | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��800 �棬��Ӧ�ﵽƽ��ʱ��NO�����ʵ���Ũ����________��

��2����ͼ�б�ʾNO2�ı仯��������________����NO2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v��________��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a. v��NO2����2v��O2������������b. ������ѹǿ���ֲ���
c. 2v����NO����v����O2�� d. �����������ƽ��Ħ���������ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ�����������________��
a. ��ʱ�����NO2���� b. �ʵ������¶�
c. ����O2��Ũ�� d. ѡ���Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��Zn��Cu�γɵ�ԭ��أ�ijʵ����ȤС������ʵ����ڶ��鿨�ϵļ�¼���£���Ƭ�������������ǣ� ��

��Cu������Zn����
��Cu���������ݲ�����������ԭ��Ӧ
��SO42-��Cu���ƶ�
������0.5mol�����������ߣ���ɲ���0.25mol����
�ݵ��ӵ������ǣ�Cu��Zn
��������Ӧʽ��Cu+2e-=Cu2+������������Ӧ��
A.�٢ڢ�B.�ڢܢ�C.�ۢܢ�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ҫ����գ���Ԫ����������ѧʽ����
�� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | �� | �� | ||||||
3 | �� | �� | �� | �� | �� | �� | �� |
��1��д������Ԫ�ص�Ԫ�ط�������___����___��
��2������ЩԪ���У�����õ�����Ԫ����___������õ�Ԫ����___��
��3������ЩԪ�ص�����������Ӧˮ�����У�������ǿ����___��������ǿ����___�������Ե�����������___��
��4��д���ۺ͢�ĵ��ʷ�Ӧ����ĵ���ʽ___��
��5��![]() C�����ڱ��е�λ�ã���___����___�壬����������ȫȼ�յIJ���ĵ���ʽ___��
C�����ڱ��е�λ�ã���___����___�壬����������ȫȼ�յIJ���ĵ���ʽ___��
��6���ڢ���ܵ������У���ѧ���ʽϻ��õ���___���жϵ�ʵ��������___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Fe[Fe(CN)6]Ϊ���������Ϳɳ�������ӵ�أ���ŵ繤��ԭ����ͼ��ʾ������˵����������

A. �ŵ�ʱ��������ӦΪFe[Fe(CN)6]+2Na++2e��=Na2Fe[Fe(CN)6]
B. ���ʱ��Mo(��)���ӵ�Դ�ĸ���
C. ���ʱ��Na+ͨ������Ĥ��������������
D. ���·��ͨ��0.2mol���ӵĵ���ʱ�����������仯Ϊ2.4g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǣ�600�� ʱ����2L�ܱ�������A��B��C�����������ܱ������з�ӦʱŨ�ȵı仯������AΪ��ɫ���壬B��C����ɫ���塣���ͼ�з�������գ�

��1���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ_____
��2����Ӧ�ﵽƽ��״̬ʱ����Ӧ���ת����Ϊ_____
��3������Ӧ���е���_____min���÷�Ӧ�ﵽƽ�⡣
��4����Ӧ�ӿ�ʼ��2����ĩ��B�����ʵ���_____����B��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊv(B)=_
��5�����������ܱ�ʾ��Ӧ��ƽ��״̬����_____����ѡ���
a.������A��B�����ʵ������
b.�������������ɫ���ٸı�
c.�����ʵ�Ũ�ȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2S2O3��5H2O����Ϊ��Ч���ȼ�����ҵ����������(FeS2)Ϊԭ���Ʊ������ʵ�������ͼ��
![]()
��֪��a.����A����ʹƷ����Һ��ɫ��������(H2S)����ܻ�õ�����
b.pHԼΪ11�������£����������������ο��Թ���������������Ρ�
�ش��������⣺
��1���������е�ԭ��B����ѡ��__(����ĸ���)��
A.NaCl��Һ B.Na2CO3��Һ C.Na2SO4��Һ
��2��ijС��ͬѧ����ͼװ��ģ���Ʊ�Na2S2O3�Ĺ���(����װ������ȥ)��

��A��ʹ��70�����������98%��Ũ���ᷴӦ���ʿ죬��ԭ����__��װ��B��������__��
��C���Ʊ�Na2S2O3������������Ӧ�У�Na2S+H2O+SO2=Na2SO3+H2S��__��Na2SO3+S![]() Na2S2O3��
Na2S2O3��
��3������ʦ����˴��������õ�����Ĺ��գ���������������ù�����ϡ�����ȡ���õ���������������壬�÷�Ӧ�Ļ�ѧ����ʽΪ__��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com