
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.86 | 1.52 | 0.66 | 1.43 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
 ,故答案为:
,故答案为: ;
;

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 物质(微粒) | 电离度α | ||||
| A | 硫酸溶液(第一步完全电离):第二步 HSO
|
10% | ||||
| B | 硫酸氢钠溶液:HSO
|
29% | ||||
| C | 醋酸:CH3COOH?CH3COO-+H+ | 1.33% | ||||
| D | 盐酸:HCl=H++Cl- | 100% |
- 4 |
- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属Na、Mg、A1熔、沸点由高到低 |
| B、HC1、HBr、HI的还原性由强到弱 |
| C、H+、Li+、H- 的半径由小到大 |
| D、同浓度的硫酸钠、醋酸钠、碳酸钠溶液的碱性由强到弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔融状态下的NaHSO4电离:NaHSO4═Na++H++SO42- |
| B、H2CO3的电离:H2CO3?2H++CO32- |
| C、Fe(OH)3的电离:Fe(OH)3?Fe3++3OH- |
| D、Na2CO3的水解:CO32-+2H2O?H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按系统命名法,有机物 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 |
| B、将1-溴丙烷和饱和氢氧化钾乙醇溶液共热,产生的气体通过酸性高锰酸钾溶液,溶液褪色,一定能证明1-溴丙烷发生了消去反应 |
C、纤维素  和壳聚糖 和壳聚糖 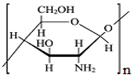 均属于多糖 均属于多糖 |
D、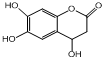 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com