
【题目】某实验室废液中含有Fe3+、Fe2+、Cu2+、Ag+四种金属阳离子,实验室设计了下述方案对废液进行处理,以回收金属,保护环境。
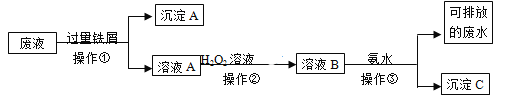
⑴沉淀A的成分是__________________________
⑵操作②中观察到的实验现象是__________________________________________________。
⑶设计一个实验方案,检验可排放的废水中不含Fe3+____________________________________________
【答案】Fe、Cu、Ag 溶液由浅绿色变黄色 取适量可排放废水于试管中,滴加硫氰化钾溶液,若无血红色出现,则不含Fe3+
【解析】
废液中含Fe3+、Fe2+、Cu2+、Ag+四种金属阳离子,操作①中加入过量的铁屑,由于铁的化学性质比铜、银活泼,因此可以把金属铜和银从盐溶液中置换出来,同时Fe3+能氧化单质铁生成Fe2+,因此在操作①得到的滤渣A中都含有金属铜、银和过量的铁,分离固体和溶液需要过滤分离,操作②滤液中加入氧化剂过氧化氢溶液氧化亚铁离子为铁离子,加入强碱溶液后生成氢氧化铁沉淀C,过滤得到可排放废液。
⑴根据以上分析可知,沉淀A的成分是Fe、Cu、Ag;
⑵操作②滤液中加入氧化剂过氧化氢溶液氧化亚铁离子为铁离子,观察到的实验现象是溶液由浅绿色变黄色;
⑶取适量可排放废水于试管中,滴加硫氰化钾溶液,若无血红色出现,则不含Fe3+。


科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.CaCl2(aq) ![]() CaCO3
CaCO3 ![]() CaO
CaO
B.Na ![]() Na2O
Na2O ![]() NaOH
NaOH
C.(C6H10O5)n(淀粉) ![]() C6H12O6(葡萄糖)
C6H12O6(葡萄糖) ![]() C2H5OH
C2H5OH
D.Cu2S ![]() Cu
Cu ![]() CuSO4
CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
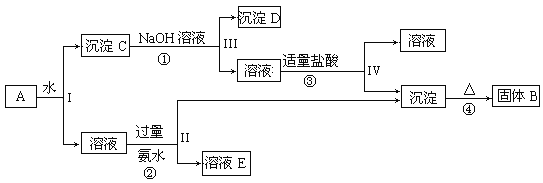
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是___________。
(2)写出①、②、③离子方程式④化学反应方程式
①____________________________;②___________________________;
③____________________________;④____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为____________________。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是_______________,1 mol 丙酮分子中含有σ键的数目为______________。
)分子中碳原子轨道的杂化类型是_______________,1 mol 丙酮分子中含有σ键的数目为______________。
(3)C、H、O 三种元素的电负性由小到大的顺序为________________。
(4)乙醇的沸点高于丙酮,这是因为____________________。
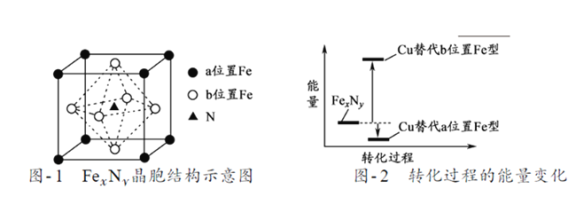
(5)某FexNy的晶胞如题21图-1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如题21图-2 所示,其中更稳定的Cu替代型产物的化学式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是单质,其中A是金属,各种物质间的转化关系如图。根据图示转化关系回答:

(1)写出下列物质的化学式。
A________,B________,甲_________,乙________。
(2)写出下列变化的化学方程式。
①A与NaOH溶液反应的化学方程式________________________________。
②甲与NaOH溶液反应的离子方程式________________________________。
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为________,转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水, 易溶于浓盐酸形成络合离子([CuCl2]-)。受潮露置空气中迅速氧化成碱式盐。实验室 用 下列流程制备:
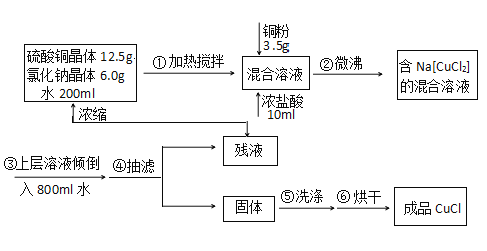
注:Na[CuCl2](易电离,溶液无色)水NaCl+CuCl↓(白色沉淀)。请回答:
(1)写出实验室制取Na[CuCl2]的离子方程式_____________。
(2)判断步骤②反应完全的现象是_______________。
(3)步骤④有关抽滤操作,下列说法正确的是_________。
A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D. 洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(4)步骤⑤用乙醇的水溶液洗涤的目的是______________。
(5)步骤⑥烘干须在真空干燥箱中进行,其原因是___________________。
(6)氯化亚铜的定量
①取样品0.25g和10ml过量的FeCl3溶液于250ml锥形瓶中,充分溶解。
②用0.10mol·L-1硫酸锶铈[Ce(SO4)2]标准溶液滴定。
已知:CuCl+FeCl3=CuCl2+FeCl2; Fe2++Ce4+=Fe3++Ce3+
三次平行试验结果如下(平行试验结果相差不能超过1%):
平行试验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(ml) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为____________。(结果保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期四种主族元素X、Y、Z、Q在周期表中的位置如图所示。X、Y、W的最外层电子数之和与Q原子核内质子数相等。下列说法中不正确的是( )
X | Y | ||
Z | Q | ||
W |
A. 离子半径![]() :r(Wm-)>r(Qm-)>r(Zn-)
:r(Wm-)>r(Qm-)>r(Zn-)
B. 元素Z和Y的化合价都可能存在![]() 价
价
C. 可以推测HWO4是W的最高价氧化物的水化物
D. X元素的氢化物种类繁多,大多可以与W元素的单质发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100molL-1NaOH溶液滴定25.00 mL 0.100molL-1H2C2O4溶液,所得滴定曲线如图所示(混合溶液的体积可看成混合前溶液的体积之和)。下列说法不正确的是( )

A. X 点所示溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)
B. 观察Y点所示溶液,说明HC2O4-的电离程度大于C2O42-的水解程度
C. Z 点所示溶液中:c(Na+)>c(C2O42-))>c(HC2O4-)>c(OH-)>c(H+)
D. 整个滴定过程中:c(Na+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.1mol·L-1的HA溶液中逐滴加入0.1mol·L-1的NaOH溶液,溶液中由水电离出H+浓度的负对数[-lgc水(H+)]与所加NaOH溶液体积关系如图所示。下列说法不正确的是
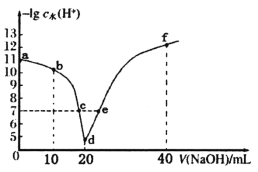
A.从a到d,HA的电离先促进再抑制
B.c、e两点溶液对应的pH=7
C.常温下,A-的水解平衡常数Kh约为1×10-9mol·L-1
D.f点的溶液呈碱性,粒子浓度之间存在:2c(HA)+c(A-)+c(H+)=c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com