
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离 子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )mol/L
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.化学反应都伴随着热量的变化
B.个别化学反应与能量变化无关
C.某些吸热反应在不加热条件下也能发生
D.放热反应的发生无需任何条件
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,m g气体A与n g气体B的分子数目一样多,下列说法不正确的是( )
A. 在任意条件下,若两种分子保持原组成,则其相对分子质量之比为m∶n
B. 25 ℃、1.25×105 Pa时,两气体的密度之比为n∶m
C. 同质量的A、B在非标准状况下,其分子数之比为n∶m
D. 相同状况下,同体积的气体A与B的质量之比为m∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.5 g锌投入100 mL 2 mol/L的稀硫酸(已知溶液密度为1.12 g/cm3)中充分反应。试计算
(1)产生的氢气在标准状况下的体积。
(2)反应后所得溶液的质量。
(3)现有2 mol/L的稀盐酸和稀硫酸各100 mL,分别加入等质量的铁,反应后生成的气体在标准状况下的体积比为2∶3,求加入铁的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成生命的化学物质中,说法不正确的是( )
A. 碳是生命的核心元素,所以在活细胞中含量最多
B. 分解脂肪比分解等量糖类物质需要消耗更多的氧气
C. 组成羽毛、肌肉、头发的主要成分是蛋白质,这些蛋白质称为结构蛋白
D. 多糖、蛋白质、核酸等物质形成过程中要脱去水分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 用括号中的试剂和方法除去各物质中的少量杂质,正确的是
A.苯中的甲苯(溴水、分液)
B.乙醇中的乙酸(NaOH溶液,分液)
C.乙醇中的水(新制CaO,蒸馏)
D.乙酸乙酯中的乙酸(NaOH溶液,分液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝Al2(OH)nCl6-n。本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
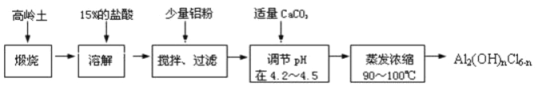
根据流程图回答下列问题:
(1)“煅烧”的目的是 。
(2)配制质量分数15%的盐酸需要200ml30%的浓盐酸(密度约为1.15g·cm-3)和 g蒸馏水,配制用到的仪器有 。
(3)“溶解”过程中发生反应的离子方程式为 。
(4)加少量铝粉的主要作用是 。
(5)“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是 。
(6)若溶解过程改为加入一定浓度的氢氧化钠溶液,发生反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器在测定稀盐酸和氢氧化钠稀溶液中和反应反应热的实验中没有使用到的是( )
①大、小烧杯 ②容量瓶 ③量筒 ④环形玻璃搅拌棒
⑤试管 ⑥温度计 ⑦蒸发皿 ⑧托盘天平
A. ①②⑥⑦ B. ②⑤⑦⑧
C. ②③⑦⑧ D. ③④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2N2O5(g)=4NO2(g)+O2(g) △H=+56.8kJ/mol自发进行的原因
A. 是吸热反应; B. 是放热反应;
C. 是熵减少的反应; D. 熵增大效应大于能量效应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com