
下列是某学生总结的一些规律,其中正确的是( )
A. 一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物
B. 酸性氧化物都可以与碱反应,生成盐和水
C. 酸根离子中不可能含有金属元素
D. 氧化物只能做氧化剂,不能做还原剂
科目:高中化学 来源: 题型:
胶体区别于其它分散系的本质特征是 ( )
A.胶体的分散质粒子能透过滤纸
B.胶体能产生丁达尔现象
C.胶体的分散质粒子直径在1~100 nm之间
D.胶体是纯净物,其它分散系是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
现有5瓶透明溶液A、B、C、D、E ,成分均是HCl、BaCl2、NaHSO4、Na2CO3、AgNO3中的一种。已知:
① A与B反应有气体生成 ② B与C反应有沉淀生成
③ C与D反应有沉淀生成 ④ D与E反应有沉淀生成
⑤ A与E反应有气体生成 ⑥ 在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式,下同)是 。
(2)A是 , C是 ,E是 。
(3)A与E反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液的说法中,正确的是
A.含H+的溶液显酸性,含OH—的溶液显碱性
B.用丁达尔现象实验可区分葡萄糖溶液和氢氧化铁胶体
C.某饱和溶液变成不饱和溶液,溶质的质量分数一定减小
D.向含有BaCl2和NaOH的混合液中通入足量的二氧化硫,最终会有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
某炼铁废渣中含有大量的CuS及少量铁的氧化物,工业上以该废渣和NaCl为原料生产CuCl2·2H2O晶体,其工艺流程中主要涉及焙烧、尾气处理、酸浸、调控溶液pH、过滤、蒸发结晶等。焙烧过程中发生的主要反应为:CuS+2NaCl+2O2 = CuCl2+Na2SO4
请回答下列问题:
(1)若最后所得的滤液中的阴离子只有SO42—和Cl—,检验滤液中这两种离子的实验操作为: ______
。
(2)焙烧时还有废气SO2产生,若在实验室中以碱液吸收处理之,下列A、B、C装置中可行的是________ (填字母);若选用甲装置,则烧杯中的下层液体可以是_______ 。
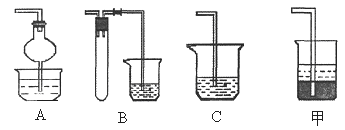 |
(3)回收SO2既能减少大气污染,又能充分利用资源。
①已知用Fe2+、Fe3+作催化剂,一定条件下在催化转化器中SO2能被O2氧化成SO42-,其中写以Fe3+为催化剂时的反应过程:
;4H++O2+4 Fe2+ === 4 Fe3+ + 2H2O
②目前国际上最先进的海水脱硫技术可对电厂尾气进行处理。这一技术的基本原理是:利用海水显弱碱性的特点,将含二氧化硫的尾气与海水、空气充分混和,最终使二氧化硫转换为硫酸盐并且不污染海水。流程图如下:
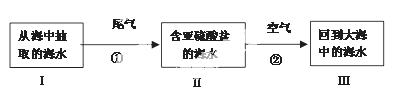
若海水I中主要阴离子为HCO3-,则反应①的离子方程式为 ;
反应②的离子方程式为 ;
检验海水Ⅲ中是否含有SO32- 所用的试剂为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知298K时,H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•mol﹣1,推测含1mol HCl的稀溶液与含1mol NH3的稀溶液反应放出的热量( )
|
| A. | 小于57.3 kJ | B. | 等于57.3 kJ | C. | 大于57.3 kJ | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI===2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________(填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是________。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式:□Al+□NaNO3+□NaOH===□NaAlO2+□N2↑+□H2O。若反应过程中转移5 mol e-,则生成标准状况下N2的体积为________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com