
某炼铁废渣中含有大量的CuS及少量铁的氧化物,工业上以该废渣和NaCl为原料生产CuCl2·2H2O晶体,其工艺流程中主要涉及焙烧、尾气处理、酸浸、调控溶液pH、过滤、蒸发结晶等。焙烧过程中发生的主要反应为:CuS+2NaCl+2O2 = CuCl2+Na2SO4
请回答下列问题:
(1)若最后所得的滤液中的阴离子只有SO42—和Cl—,检验滤液中这两种离子的实验操作为: ______
。
(2)焙烧时还有废气SO2产生,若在实验室中以碱液吸收处理之,下列A、B、C装置中可行的是________ (填字母);若选用甲装置,则烧杯中的下层液体可以是_______ 。
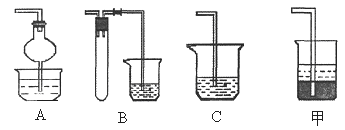 |
(3)回收SO2既能减少大气污染,又能充分利用资源。
①已知用Fe2+、Fe3+作催化剂,一定条件下在催化转化器中SO2能被O2氧化成SO42-,其中写以Fe3+为催化剂时的反应过程:
;4H++O2+4 Fe2+ === 4 Fe3+ + 2H2O
②目前国际上最先进的海水脱硫技术可对电厂尾气进行处理。这一技术的基本原理是:利用海水显弱碱性的特点,将含二氧化硫的尾气与海水、空气充分混和,最终使二氧化硫转换为硫酸盐并且不污染海水。流程图如下:
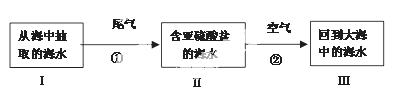
若海水I中主要阴离子为HCO3-,则反应①的离子方程式为 ;
反应②的离子方程式为 ;
检验海水Ⅲ中是否含有SO32- 所用的试剂为 。
科目:高中化学 来源: 题型:
反应 H2(g) + I2(g)  2HI(g)的平衡常数K1 ,反应 HI(g)
2HI(g)的平衡常数K1 ,反应 HI(g) 
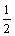 H2(g)+
H2(g)+ 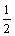 I2(g)的
I2(g)的
平衡常数K2 ,则K1、K2的关系为(平衡常数为同温度下的测定值)
A.K1=2K2 B.K1=K22 C.K1=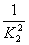 D.K1=
D.K1=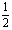 K2
K2
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应:①2C-+A2===2A-+C2;②2B-+D2===2D-+B2;③2A-+B2===2B-+A2。推断A-、B-、C-、D-的还原能力由强到弱的顺序是 ( )
A.A->B->C->D-
B.D->B->A->C-
C.D->A->B->C-
D.C->A->B->D-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某学生总结的一些规律,其中正确的是( )
A. 一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物
B. 酸性氧化物都可以与碱反应,生成盐和水
C. 酸根离子中不可能含有金属元素
D. 氧化物只能做氧化剂,不能做还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A、高温下FeSO4发生如下反应:2FeSO4高温Fe2O3+SO2↑+SO3↑,将生成的气体通入氯化钡溶液中,得到的沉淀物是BaSO3和BaSO4
B、浅绿色的Fe(NO3)2溶液中存在着如下的平衡:Fe2++2H2O Fe(OH)2+2H+
Fe(OH)2+2H+
若在此溶液中加入盐酸,则Fe2+浓度增大
C、在铁和铜的混合物中,加入不足量的稀硝酸,反应后剩余金属m1g;再向其中加入一定量的稀硫酸,充分振荡后 ,剩余金属m2g,则m1大于等于m2
D、实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取的Na2CO3质量分别为1000mL , 212.0g。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如下图(反应条件及其它产物已略去)。
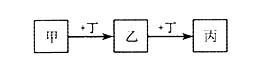
下列说法不正确的是
A.若甲是AlCl3溶液,则丁可能是NaOH溶液
B.若甲是Fe,则丁可能是Cl2
C.若丁是CO2,则甲可能为Mg
D.若丁是O2,则乙、丙的相对分子质量可能相差16
查看答案和解析>>
科目:高中化学 来源: 题型:
【[化学—有机化学基础】没食子酸丙酯简称PG,结构简式为 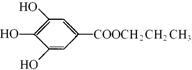 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
⑴PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
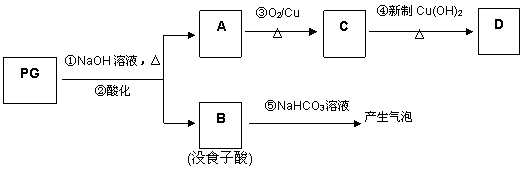 PG可发生如下转化:
PG可发生如下转化:
⑵A的结构简式为 ,1mol没食子酸最多可与 mol H2 加成。
⑶上图的有关变化中,属于氧化反应的有(填序号) 。
⑷从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
a.含有苯环 b.含有羧基 c.含有酚羟基 d. 微溶于食用油
⑸反应④的化学方程式为:
⑹B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:
i.含有苯环,且苯环上的一溴代物只有一种;ii.既能发生银镜反应,又能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
|
| A. | 溴水中有下列平衡Br2+H2O═HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
|
| B. | 合成氨反应(正反应为放热反应),为提高氨的产率,理论上应采取降低温度的措施 |
|
| C. | 反应CO(g)+NO2(g)═CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
|
| D. | 对于2HI(g)═H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA 表示阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,0. 1 mol Cl2 溶于水,转移的电子数目为0. 1NA
B.常温常压下,18 g H2O 中含有的原子总数为3NA
C.标准状况下,11. 2 L CH3CH2OH 中含有的分子数目为0. 5NA
D.常温常压下,2. 24 L CO 和CO2 混合气体中含有的碳原子数目为0. 1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com