
����Ŀ��ij��ѧС����̽�������仯����������Ժͻ�ԭ�ԣ���ش��������⣺
(1)����ͷ�ι��⣬����Ϊ��ʵ��ز���ȱ�ٵ�һ�ֲ���������___________��
(2)��������������ʵ�鱨�棺
ʵ��Ŀ�ģ�̽�������仯����������Ժͻ�ԭ�ԡ�
�Լ������ۡ�FeCl3��Һ��FeCl2��Һ����ˮ��пƬ��ͭƬ��
ʵ���¼(��б�߲��ֲ�����д)��
��� | ʵ������ | ʵ������ | ���ӷ���ʽ | ʵ����� |
�� | ��FeCl2��Һ�е���������ˮ | ��Һ��dz��ɫ��Ϊ�ػ�ɫ | Fe2+���л�ԭ�� | |
�� | ��FeCl2��Һ�м���пƬ |
| Zn��Fe2+��Zn2+��Fe | |
�� | ��FeCl3��Һ�м����������� |
| Fe��2Fe3+��3 Fe2+ | Fe3+���������� |
�� |
|
| Fe3+���������� |
ʵ����ۣ�_________________________________��
(3)�������Ͻ����жϣ����������м��������ԣ����л�ԭ�Ե��У�_____��(�����)
A��Cl2 B��Na C��Na+ D��Cl�� E��SO2 F������
���𰸡��Թ� Cl2��2Fe2+��2Cl����2Fe3+��Fe2+�����������������ܽ⣬��Һ���ػ�ɫ��Ϊdz��ɫ����FeCl3��Һ�м���ͭƬ Cu+2Fe3+= Cu2++2Fe2+ʵ����ۣ�Feֻ�л�ԭ�ԣ�Fe3+ֻ�������ԣ�Fe2+���������ԣ����л�ԭ�ԡ� A E F
��������
��1����������ʵ����ȡ�����Լ����з�Ӧ�����ݷ�Ӧ��������ж��������ʣ�ʵ�������Թ��н�����
��2����.�Ȼ�������Һ�м�����ˮ����Һ��dz��ɫ��Ϊ�ػ�ɫ����Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
��.�Ȼ�������Һ����пƬ��пƬ�ܽ⣬���������������ӱ���ԭ��֤���������Ӿ��������ԣ�
��.�����ӷ���ʽ��֪��ʵ������Ϊ�������ܽ⣬��Һ���ػ�ɫ��Ϊdz��ɫ��
��.��FeCl3��Һ�м���ͭƬ����Ӧ�����Ȼ��������Ȼ�ͭ�����ӷ�ӦΪCu+2Fe3+=2Fe2++Cu2+��FeCl3��FeԪ�صĻ��ϼ۽��ͣ����˵��Fe3+���������ԣ�
ʵ����ۣ�Feֻ�л�ԭ�ԣ�Fe3+ֻ�������ԣ�Fe2+���������ԣ����л�ԭ�ԡ�
��3��Ԫ�ػ��ϼۿ�������Ҳ���Խ��͵ļ��������ԣ����л�ԭ�ԣ�
A.Cl2����Ԫ�ػ��ϼۿ�������Ϊ+1�ۣ�Ҳ���Խ���Ϊ-1�ۣ�˵���Ⱦ���������Ҳ���л�ԭ�ԣ���A��ȷ��
B.Na�ǽ���ֻ��ʧ���Ӿ��л�ԭ�ԣ���B����
C.Na+Ԫ�ػ��ϼ�ֻ�ܽ��ͣ�����Ϊ�����ԣ���C����
D.Cl-Ԫ�ػ��ϼ۴�����ͼۣ����ϼ�ֻ�����߱��ֻ�ԭ�ԣ���D����
E.SO2����Ԫ�ػ��ϼۿ�������Ϊ+6�ۣ�Ҳ���Խ���Ϊ-2�ۣ�����Ϊ�����Ժͻ�ԭ�ԣ���E��ȷ��
F.HCl����Ԫ�ػ��ϼ�Ϊ��ͼۣ��ܹ����ֻ�ԭ�ԣ���Ϊ��ۣ��ܱ��������ԣ��ʻ�����μӷ�Ӧʱ���ɱ���Ϊ�����Ժͻ�ԭ�ԣ���F��ȷ��
�ʴ�Ϊ��AEF��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����
A. 1mol ������ˮ������ȫ��Ӧת�Ƶĵ�����Ϊ3NA
B. ���³�ѹ�£�1mol �������е�ԭ����ΪNA
C. ��״���£�11. 2 L �Ҵ����еķ�����ĿΪ0. 5NA
D. ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl- ����Ϊ NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҷ�ȩ(OHC-CHO)��ѧ���ʻ��ã��Ƿ�֯��ҵ�г��õ�һ���л�ԭ�ϣ�������������������ά�ķ����Ժͷ����ԡ��乤ҵ����������Ҫ���Ҷ���(HOCH2CH2OH)���������������ȩҺ����������������ش������������:
(1)�Ҷ��������������
���Ҷ���������Ϊԭ�ϣ��ڴ������ڵ������£�250�����ҿ�ʼ�������У������Ҷ�ȩ�������Ҵ���[CH2(OH)COOH]�ķ�Ӧ����ʽ:
I.HOCH2CH2OH(g)+O2(g) ![]() OHC-CHO(g)+2H2O(g)��H1
OHC-CHO(g)+2H2O(g)��H1
II.HOCH2CH2OH(g)+O2(g) ![]() CH2(OH)COOH(g)+H2O(g)��H2
CH2(OH)COOH(g)+H2O(g)��H2
��֪��ӦI����ػ�ѧ��������������:
��ѧ�� | C-H | C-O | H-O | O==O | C==O | C-C |
E/kJ��mol-1 | 413 | 343 | 465 | 498 | 728 | 332 |
�١�H1=_____kJ/mol����ӦI�Ļ�ѧƽ�ⳣ������ʽΪK=________��
�������I��ƽ����ʣ����Բ�ȡ�Ĵ�ʩ��______(����)��
A.�����¶� B.����ѹǿ C.�����¶� D.��Сѹǿ
������Ҷ�ȩ��Ӧѡ���ԵĹؼ�������_________________________��
�ܱ����¶Ⱥ��ݻ����䣬����������˵����ӦI�ﵽƽ��״̬����________(����)��
A.v��(O2)=2v��(H2O)
B.��������ѹǿ������ʱ��仯���仯
C.���������ܶȲ��ٷ����仯
D.�Ҷ�����OHC-CHO�����ʵ���֮��Ϊ1:1
E.����������Ҷ�ȩ������������ٷ����仯
(2)��ȩ(CH3CHO)Һ������������
11.0g40%����ȩ��Һ��40%�����ᣬ��һ������Ͷ��������Ӧ���ڣ���Cu(NO3)2���£������¶���38��40��ʱ����Ӧ10h����ͨ����ȡ�Ȳ�����ȥ��ȩ������ȣ����ѹŨ����4.35g40%�Ҷ�ȩ��Һ��
����ϡ����������ȩ��ȡ�Ҷ�ȩʱ����N2O�������仯ѧ����ʽΪ______________________��
�������������ݣ������Ҷ�ȩ�IJ���Ϊ___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10mL��0.1mol/L��NaOH��Һ�м���0.1mol/L��HA��Һ����ҺpH�ı仯������ͼ��ʾ������˵����ȷ����( )
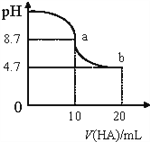
A. pH=7ʱ��c(Na+)= c(A-)��c(HA)
B. a����ʾ��Һ��c(Na+)��c(A-)��c(H+)��c(HA)
C. b����ʾ��Һ����c(A-)��c(HA)
D. a��b������ʾ��Һ��ˮ�ĵ���̶���ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��Ϊ�о��绯ѧԭ���������ͼװ��������������ȷ����( )
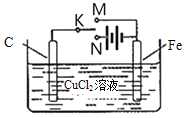
A. K��M����ʱ��ÿת��1mol����Fe��������32gCu
B. K��N����ʱ��̼���ϲ���ʹʪ��ĵ���-KI��ֽ����������
C. K�ֱ���M��N����ʱ�������ܵ�����
D. K��M��N���Ͽ���һ��ʱ���������Һ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������6����Ӧ����Ӧ�����ԣ���
A.2Na+2H2O �T2NaOH+H2�� B��CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
C��KClO3![]() 2KCl+3O2�� D��CaCO3+2HCl�TCaCl2+H2O+CO2��
2KCl+3O2�� D��CaCO3+2HCl�TCaCl2+H2O+CO2��
E��Na2O+CO2 �TNa2CO3 F��CO2+C![]() 2CO
2CO
�����ڻ��Ϸ�Ӧ������������ԭ��Ӧ����__________�����ţ���ͬ����������������ԭ��Ӧ����__________��
��2�����ݷ�Ӧ����2Fe3����2I��===2Fe2����I2����Br2��2Fe2��===2Fe3����2Br������ Br2��2I��===I2��2Br�����ش��������⡣
�����ж����ӵĻ�ԭ����ǿ������˳����________
A��Br����Fe2����I�� B��I����Fe2����Br�� C��Br����I����Fe2�� D��Fe2����I����Br��
��ij��Һ�к���Br����Fe2����I����Ϊ������I������Ӱ��Br����Fe2����ѡ�õ���������__________��
��I2��Br���ܷ�����Ӧ________
A.�� B.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�̽��ͭ��ϡHNO3����Ӧ�������£�
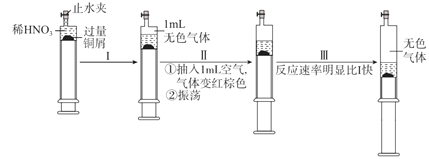
����˵������ȷ����
A. ����I��������ɫ��������ӷ���ʽ��3Cu+2 NO3-+8H+ =3Cu2++2NO��+4H2O
B. ����III��Ӧ���ʱ�I���ԭ����NO2����ˮ��ʹc(HNO3)����
C. ��ʵ���֪��NO2�Ը÷�Ӧ���д�����
D. �����������ƶ�ʱ���ٳ��������ͭ���Լ����ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0. 10 mol��L-1��Na2CO3��Һ����μ���ϡ���ᣬ�����HCl��ԭ��Һ��Na2CO3�����ʵ���֮��f[f=![]() ]����ҺpH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
]����ҺpH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
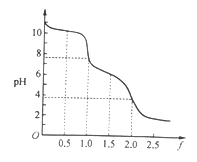
A. f=0ʱ����Һ�У�c(Na+)=2c(CO32-)
B. f=0.5ʱ����Һ�У�c(HCO3-)>c(CO32-)
C. f= 1ʱ����Һ�У�c(Na+) + c(H+) = 2c(CO32-) + c(HCO3-)+c(OH-)
D. f=2ʱ����Һ�У�1/2c(Na+)=c(CO32-)+c( HCO3-)+c(H2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧʽ��ȷ����
A. Ǧ���س��ʱ�����ķ�Ӧʽ:Pb2++2e-=Pb
B. ����п�̸ɵ�طŵ�ʱ��������Ӧʽ:Zn-2e-=Zn2+
C. ���Ը�������������Һ:2MnO4-+5C2O42-+16H+=2Mn2++10CO2��-8H2O
D. I�����軯�ؼ���Fe2+:3FeCl2+2K3[Fe(CN)6]=Fe3[Fe(CN)6]2��+6KCl
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com