


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 物质 | 颜色和状态 | 密度/g?cm3 | 0℃时溶解度/g | 100℃时溶解度/g |
| KCl | 无色晶体 | 1.98 | 27.6 | 56.7 |
| KClO3 | 无色晶体 | 2.32 | 3.3 | 57 |
| KClO4 | 无色晶体 | 2.32 | 0.75 | 21.8 |
| 1 |
| 3 |
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
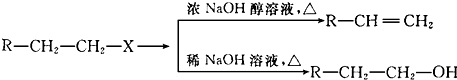
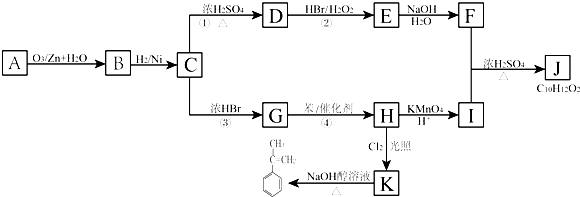
 合成
合成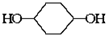 .(部分试剂和反应条件已略去)
.(部分试剂和反应条件已略去)
查看答案和解析>>
科目:高中化学 来源: 题型:
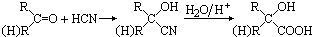 ,CO和H2按物质的量之比1:2可以制得G,有机玻璃可按如图路线合成:
,CO和H2按物质的量之比1:2可以制得G,有机玻璃可按如图路线合成: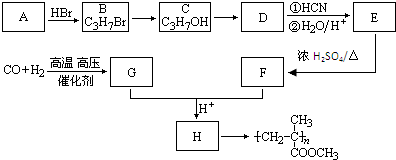
查看答案和解析>>
科目:高中化学 来源: 题型:
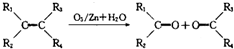 (其中R、R1、R2、R3和R4均表示烃基)
(其中R、R1、R2、R3和R4均表示烃基)查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径(10-10m) | 1.30 | 0.82 | 0.99 | 1.11 | 0.90 | 1.18 |
| 最高或最低化合价 | +2 | +3 | +7 | +4 | +2 | +3 |
| -1 | -4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素原子的最外层电予数等于元素的最高化合价 |
| B、电子层数相同的主族元素,最外层电子数多的原子半径小 |
| C、K、Mg、Al失电子能力和最高价氧化物水化物的碱性均依次增强 |
| D、第三周期元素中,最外层电子数≥电子层数的为非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A>B>C |
| B、A>C>B |
| C、B>A>C |
| D、B>C>A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com