
【题目】已知:X(g)+2Y(g)![]() 3Z(g) △H=-a kJ.mol-1(a>0)。下列说法不正确的是
3Z(g) △H=-a kJ.mol-1(a>0)。下列说法不正确的是
A. 升高反应温度,逆反应速率增大,正反应速率增大
B. 达到化学平衡状态时,X、Y、Z的质量不再发生变化
C. 达到化学平衡状态时,反应放出的总热量可达akJ
D. X和Y充分反应生成Z的物质的量不可能达到3 mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50mol/L NaOH溶液

(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体___g。
(2)从表中选择称量NaOH固体所需要的仪器是(填字母):___。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(1)写出该反应的热化学方程式(中和热为57.3kJ/mol):___。
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表:
①请填写下表中的空白:
| 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
2 | 27.0 | 27.4 | 27.2 | 31.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.3 | |
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃)。则中和热△H=___(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)___。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述不正确的是

A. 当溶液pH=4.6时c(HX-)>c(X2-)
B. 当 时溶液中c(HX-)=c(H2X)
时溶液中c(HX-)=c(H2X)
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时:c(Na+)> c(HX-)> c(X2-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应与能量的说法中错误的是( ) 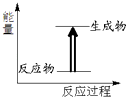
A.如图所示的反应为放热反应
B.化学反应中有物质变化也有能量变化
C.需要加热的化学反应不一定是吸热反应
D.化学键断裂吸收能量,化学键生成放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柔性电子产品因具有独特的柔性、延展性等优点在信息、医疗、能源等领域具有广泛应用前景。下图为中科院张新波课题组受中国传统书法艺术启发,直接将用毛笔书写后的纸张和锂箔作为电极材料组装成的锂空气电池。下列说法不正确的是( )

A. 纸张电极是该电池的正极
B. 锂箔电极发生的电极反应:Li﹣e-=Li+
C. 电池工作时,电子从锂箔电极经导线流向纸张电极,再从纸张电极经电解质溶液流向锂箔电极
D. 该电池具有轻型、柔性且可折叠的特点,有望应用于柔性电子器件
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某矿物固体X(仅含4种短周期元素)的组成和性质,其中固体乙可制光导纤维。现设计并完成如下实验:

请回答:
(1)X除了含有H、O元素以外还含有____________。
(2)固体丙的用途____________。
(3)X的化学式是____________。
(4)固体乙与NaOH溶液反应的离子方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要证明某溶液中不含Fe3+,而可能含有Fe2+,合理的操作顺序是( )
①加入足量的氯水 ② 取少量试液 ③加入少量KSCN溶液
A. ①③② B. ③②① C. ②③① D. ②①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com