
【题目】下列判断正确的是 ( )
A.在稀氨水中加水稀释,![]() 会增大
会增大
B.若酸性HA>HB,则等物质的量浓度等体积的NaA和NaB溶液混合有关系: c(OH-)>c(A-)>c(B-)>c(H+)
C.0.1 mol·L-1的一组溶液pH由大到小排列为: NaOH>Na2CO3>NaHSO4>(NH4)2SO4
D.分别稀释10mLpH=1的盐酸和醋酸至100mL,后者pH变化大,说明醋酸是弱酸
【答案】A
【解析】
A.溶液越稀越电离,弱电解质的电离程度增大;
B.弱离子水解时,生成的弱酸酸性越弱,则水解程度越大;
C.硫酸氢钠在水溶液中完全电离出三种离子:钠离子,氢离子和硫酸根离子;
D.弱酸稀释中会促进弱酸的电离。
A.溶液越稀越电离,加水稀释氨水,会使电离平衡右移, ![]() 会增大,故正确;
会增大,故正确;
B.弱离子水解时,生成的弱酸酸性越弱,则水解程度越大,酸性HA>HB,说明NaB溶液中阴离子的水解程度大于NaA中阴离子的水解程度,所以c(A-)>c(B-),氢氧根是弱离子水解生成的,其浓度比弱的阴离子的小,所以离子浓度关系: c(A-)>c(B-)>c(OH-)>c(H+),故错误;
C. 氢氧化钠完全电离,溶液显强碱性,碳酸钠水解显碱性,硫酸氢钠在水溶液中完全电离出三种离子:钠离子,氢离子和硫酸根离子,溶液显强酸性,硫酸铵水解显酸性,所以pH由大到小排列为:NaOH> Na2CO3>(NH4)2SO4>NaHSO4,故错误;
D. 盐酸是强酸,醋酸是弱酸,弱酸稀释中会促进弱酸的电离, 稀释10mLpH=1的盐酸至100mL,pH=2;稀释10mLpH=1的醋酸至100mL,pH小于2;错误;
综上所述,本题正确选项A。


科目:高中化学 来源: 题型:
【题目】与下列事实对应的化学用语错误是( )
A.纯碱溶液能清洗油污:CO32﹣+H2OHCO3﹣+OH﹣
B.配制FeSO4溶液时加入适量的铁粉:Fe3++Fe→2Fe2+
C.含1molNaOH和1molNa2CO3的混合溶液中滴入含1.5molHCl的稀盐酸:2OH﹣+CO32﹣+3H+→HCO3﹣+2H2O
D.NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42﹣恰好沉淀完全:2Ba2++4OH﹣+Al3++2SO42﹣→2BaSO4↓+AlO2﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的各图中,表示2A(g)+B(g)2C(g)(△H<0)这个可逆反应的正确图象为(注:(C)表示C的质量分数,P表示气体压强,C表示浓度)
A. B.
B.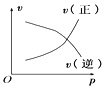 C.
C.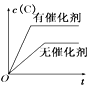 D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成是一个需要经历多步反应的过程,我们常用的塑料包装绳(主要成分为聚氯乙烯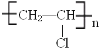 就是通过多步反应生产出来的。现在有1,2-二溴乙烷,氢氧化钠醇溶液、二氧化锰、锌粒、稀硫酸等主要原料,请您设计反应的步骤得到聚氯乙烯,将每一步反应的化学方程式写出__________________________________
就是通过多步反应生产出来的。现在有1,2-二溴乙烷,氢氧化钠醇溶液、二氧化锰、锌粒、稀硫酸等主要原料,请您设计反应的步骤得到聚氯乙烯,将每一步反应的化学方程式写出__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HA![]() H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向________(填“正”、“逆”)反应方向移动,理由是________ 。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向______(填“正”、“逆”)反应方向移动,溶液中c(A-)将________(填“增大”、“减小”或“不变”),溶液中c(OH-)将________(填“增大”、“减小”或“不变”)。
(3)在25 ℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_______性(填“酸”、“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四瓶丢失标签的NaOH、Na2CO3、AlCl3、NH4HSO4溶液,为鉴别四瓶溶液,将四瓶溶液编号为A、B、C、D进行实验。实验过程和记录如下图所示(无关物质已经略去):
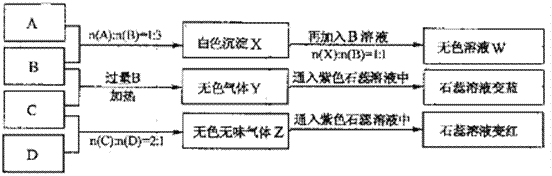
请回答:
(1)A、W的溶液分别加热蒸干并灼烧最后所得固体为_______、_______。
(2)D溶液pH__(填“大于”、“小于”或“等于”)7,原因是(用离子方程式表示)__________。
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是________________。(用化学式表示)
(4)等物质的浓度的C溶液与NH4Cl溶液相比较,c(NH4+):前者____后者(填“<”“>”“=”)。
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是______________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用以下图示装置研究物质的性质,能够获得可靠结论的是
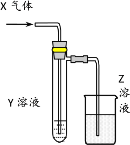
X | Y | Z | 结论 | |
A | HCHO | 新制Cu(OH)2 | NaOH(aq) | 验证甲醛的还原性 |
B | CH3Cl | AgNO3(aq) | NaOH(aq) | 验证一氯甲烷含氯元素 |
C | SO2 | KMnO4(aq) | NaOH(aq) | 验证二氧化硫的漂白性 |
D | Cl2 | 淀粉KI(aq) | NaOH(aq) | 验证氯气的强氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种芳香族化合物A,其蒸气密度是相同条件下H2密度的82倍,A由碳、氢、氧三种元素组成,经测定碳、氢的质量分数分别为73.2%和7.32%。
(1)A的分子式是__;
(2)已知:
ⅰ.![]() (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
ⅱ.![]()
又知,A在一定条件下能发生如下转化,某些生成物(如H2O等)已略去.

请回答:
①步骤Ⅰ的目的是__;
②若G为气体,且相对分子质量是44,则E的结构简式是__;E的核磁共振氢谱中有__个吸收峰(填数字);
③F→H的反应类型是__;
④F在一定条件下可发生酯化反应,生成M(M与FeCl3反应,溶液呈紫色;且分子结构中含有苯环和一个七元环)请写出该反应的化学方程式__;
⑤A的结构简式是__;
上述转化中B→D的化学方程式是__;
(3)已知A的某种同分异构体K具有如下性质:
①K与FeCl3反应,溶液呈紫色
②K在一定条件下可发生银镜反应
③K分子中苯环上的取代基上无甲基
请写出K所有可能的结构简式__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com