
【题目】下列叙述中所描述的物质一定是金属元素的是( )
A. 易失去电子的物质
B. 原子最外电子层只有一个电子的元素
C. 单质具有金属光泽的元素
D. 原子的最外电子层只有2个电子且核外电子总数大于3的元素
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】已知氯酸钠(NaClO3)与盐酸反应的化学方程式为NaClO3+6HCl===NaCl+3Cl2↑+3H2O,则氧化产物和还原产物的质量比为( )
A. 6∶1 B. 5∶1 C. 3∶1 D. 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Na、Na2O,Na2O2的混合物与足量的水反应,在标准状况下得到672mL混合气体,将混合气体通电后恰好完全反应,则Na、Na2O,Na2O2的物质的量之比为( )
A.4:3:2
B.1:2:1
C.2:1:1
D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)=CO2(g) ΔH1 C(s)+![]() O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+![]() O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO+H2O(l)===Ca(OH)2(s) ΔH8
A. ①③④ B. ②③④ C. ①④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在酸性条件下有以下反应关系:
(i)KBrO3能将KI氧化成I2或KIO3 , 其本身被还原为Br2 .
(ii)Br2能将I-氧化为I2 .
(iii)KIO3能将I-氧化为I2 , 也能将Br-氧化为Br2 , 其本身被还原为I2 .
①上述物质中氧化剂氧化能力由强到弱的顺序是 .
②现向含有1molKI的硫酸溶液中加入含amolKBrO3的溶液,a的取值范围不同,所得产物也不同.试将讨论的结果填入下表.
编号 | a的取值范围 | 产物的化学式或(离子符号) |
A | I2 , Br- | |
B |
| |
C | a= | |
D | I2 , IO3- , Br2 | |
E | a≥ |
③若产物中碘单质和碘酸钾的物质的量相等,a的值为 .
④若a的值为1时,其产物及其物质的量分别为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s) + O2(g) = CO2(g);ΔH = -393.15 kJ·mol-1 ①
途径Ⅱ 先制成水煤气:
C(s) + H2O(g) = CO(g) + H2(g); ΔH2 ②
再燃料水煤气:
2CO(g) + O2(g) = 2CO2(g); ΔH= -566kJ·mol-1 ③
2H2(g) + O2(g) = 2H2O(g);ΔH= -484 kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上_________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH2=_______________。
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为
NO(g)+O3(g)==NO2(g)+O2(g) ΔH=-200.9kJ·mol-1
NO(g)+![]() O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
SO2(g)+O3(g)==SO3(g)+O2(g) ΔH=-241.6kJ·mol-1
反应3NO(g)+O3(g)==3NO2(g)的ΔH=________kJ·mol-1。
(4)已知下列各组热化学方程式
① Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 △H=-25kJ/mol
② 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③ Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式______________________________。
(5)在标准状况下的11.2L甲烷完全燃烧生成CO2 和液态水放出444.8kJ热量(298K),其燃烧热的热化学方程式______________________________________________________; 已知断裂下列1mol化学键需要吸收的能量分别为:C=O:745kJ/mol , O=O:496kJ/mol , C-H:414kJ/mol 则断裂1molH-O键需要提供的能量为____________________ kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于金属钠的性质描述不正确的是( )
A. 很软可用刀切割 B. 在空气中燃烧生成白色的过氧化钠
C. 金属钠通常保存在煤油里 D. 钠具有银白色金属光泽,密度比水小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长托宁是一种选择性抗胆碱药,可通过以下方法合成(部分反应条件略去):
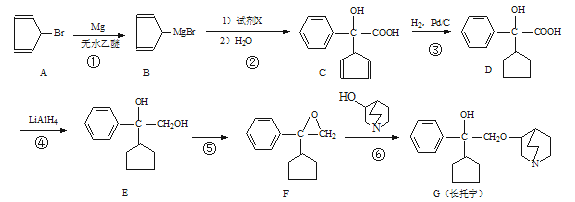
(1)长托宁中的含氧官能团为_________和_________(填名称)。
(2)反应②中加入试剂X的分子式为C8H6O3 ,X的结构简式为________。
(3)反应③的反应类型为_______________。
(4)C的一种同分异构体满足下列条件:
I.能与FeCl3溶液发生显色反应。
II.核磁共振氢谱有5个峰且峰的面积比为2:4:4:1:1;分子中含有两个苯环。写出该同分异构体的结构简式:_________________。
(5)根据已有知识并结合相关信息,写出以![]() 和
和![]() 为原料制备
为原料制备![]() 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:_______________
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:_______________
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com