
【题目】下列离子方程式正确的是( )
A. NaHS溶于水: NaHS = Na+ + H+ + S2-
B. Al(OH)3电离: H2O+AlO2-+H+=Al(OH)3=Al3++3OH-
C. NaHSO4溶于水:NaHSO4=Na++ HSO4-
D. HF溶于水:HF+H2O![]() H3O++F-
H3O++F-
科目:高中化学 来源: 题型:
【题目】碳及化合物在生产生活中用比较广泛。回答下列问题:
(1)已知:①H2(g)+ ![]() O2(g)=H2O(1)△H1=-285.8kJ·mol-1
O2(g)=H2O(1)△H1=-285.8kJ·mol-1
②CH3OH(1)+ ![]() O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1
O2(g)=CO2(g)+2H2O(1) △H2=-725.5kJ·mol-1
则CO2(g)+3H2(g)=CH2OH(1)+H2O(1)的反应热 △H=____________。
(2)某研究小组用CO合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
CH3OH(g)△H<0,将三组混合气体分别通入到三个2L恒容密闭容器中进行反应,得到如下三组实验数据:
实验组 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | 达到平衡所需的时间/min | ||||
CO | H2 | CH3OH | CO | H2 | CH3OH | |||
1 | 650 | 2.0 | 6.0 | 0 | 1.0 | 5 | ||
2 | 900 | 2.0 | 6.0 | 0 | 1.2 | 2 | ||
3 | 650 | 1.0 | 4.0 | 2.0 | a | b | c | t |
实验1条件下平衡常数K=__________,a、b之间可能的关系为_____________。
已知反应CO(g)+2H2(g)![]() CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:
CH3OH(g)中CO的转化率(a)与温度(T)、压强(p)的关系如右图所示:

①p1______p2(填“<”“>”“=”)。先升高温度、后增大压强,能否实现b点到c点的转化?__________(填“能”或“不能”),原因是_____________________________________________。
②a、c两点的反应速率为v1________v2(填“<”“>”“=”)。
③在不改变反应物用量情况下,为提高CO的转化率可采取的措施是_____________(答出三条措施)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题。
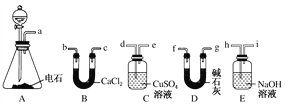
(1)A中制取乙炔的化学方程式为_________________________________。
(2)制乙炔时,旋开分液漏斗的活塞,使水慢慢滴下的原因是_________________。
(3)用电石制得的乙炔中常含有H2S、PH3等杂质,除去杂质应选用________(填序号,下同)装置,干燥乙炔最好选用________装置。
(4)为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:
纯净乙炔气![]() 混合液
混合液![]() 有机混合物Ⅰ
有机混合物Ⅰ![]() 混合液
混合液![]() 有机混合物Ⅱ
有机混合物Ⅱ
①操作b的名称是________;
②有机混合物Ⅰ可能含有的物质是________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲苯可以进行如下转化:

回答下列问题:
(1)反应①的反应类型为__________,反应③的反应类型为_____________。
(2)化合物A的结构简式为____________。化合物D的分子式为_____________。
(3)反应②的化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式,标出电子转移的方向和数目:
![]()
_______________________________________
(2)整个反应过程中的还原剂是__________、___________。
(3)把KI换成KBr,则CCl4层变为橙红色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是________________。据此请判断下列反应能否进行:HBrO3 +HCl → Br2 + Cl2 + H2O(未配平)_________(填“能”或“否”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列说法正确的是
A. 1 mol羟基中含有l0NA个电子
B. 常温下,22.4 L CH4在O2中完全燃烧,生成NA个CO2分子
C. 标准状况下,18 g H2O中所含的氧原子数为NA
D. 0.2 mol L-1的NH4Cl溶液中含有0.2NA个NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com