
A、新药帕拉米韦对禽流感H7N9有显著疗效,它的结构简式为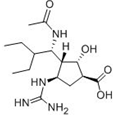 化学式是C15H26N4O4 化学式是C15H26N4O4 |
| B、2013年11月20日山东现‘夺命快递’----化学品泄漏致1死7中毒.该化学品为氟乙酸甲酯它是无色透明液体,溶于乙醇、乙醚,不溶于水.它属于酯类,也属于卤代烃 |
C、绿原酸的结构简式为: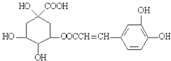 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 |
D、苯的同系物 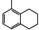 ,其所有碳原子不可能在同一平面上 ,其所有碳原子不可能在同一平面上 |
 与苯的不饱和度不同,且分子中存在4个亚甲基,均为四面体构型.
与苯的不饱和度不同,且分子中存在4个亚甲基,均为四面体构型. 与苯的不饱和度不同,则不是苯的同系物,且分子中存在4个亚甲基,均为四面体构型,所有的C不可能共面,故D错误;
与苯的不饱和度不同,则不是苯的同系物,且分子中存在4个亚甲基,均为四面体构型,所有的C不可能共面,故D错误;

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源: 题型:
| A、该分子中既含有极性共价键,又含有非极性共价键 |
| B、该分子是极性分子 |
| C、该分子中六个原子位于同一平面,键角为120° |
| D、该物质难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5作为空气质量预报的一项重要指标,它是指空气中直径大于或等于2.5μm的颗粒物,该值越高,代表空气污染程度越严重 |
| B、新型材料聚酯纤维、光导纤维都属于有机高分子 |
| C、上海世博会很多展馆采用光电转化装置,体现当今“低碳”经济的理念 |
| D、塑化剂是一种化工塑料软化剂,可以大量添加到婴幼儿玩具中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OH-+CO32-+2H+→HCO3-+H2O |
| B、2OH-+CO32-+3H+→HCO3-+2H2O |
| C、2OH-+CO32-+4H+→CO2↑+3H2O |
| D、OH-+CO32-+3H+→CO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
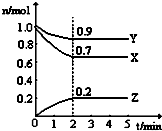 某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,H2、N2、NH3三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
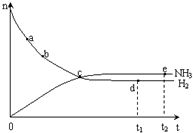 合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0
合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:
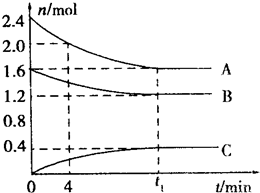 T℃时,在一容积为2L的容器中,A气体和B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示:
T℃时,在一容积为2L的容器中,A气体和B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com