
| A、HCl |
| B、CuCl2 |
| C、Na2SO4 |
| D、CuSO4 |
| ||


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
| A、还原性:Na>Mg>Al>Fe |
| B、碱性:Al(OH)3>Mg(OH)2 |
| C、稳定性:HF>HCl>HBr>HI |
| D、酸性:HClO4>H2SO4>CH3COOH>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3HCl+Fe(OH)3═FeCl3+3H2O |
| B、HNO3+KOH═KNO3+H2O |
| C、H2SO4+Ba(OH)2═BaSO4↓+2H2O |
| D、2HCl+Cu(OH)2═CuCl2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
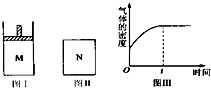 在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ)中,分别加入a mol A和a mol B,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?xC(g)△H<0,平衡时M中A、B、C的物质的量之比为1:3:4,下列判断不正确的是( )
在恒压密闭容器M(如图Ⅰ)和恒容密闭容器N(如图Ⅱ)中,分别加入a mol A和a mol B,起始时两容器体积均为V L,发生如下反应并达到化学平衡状态:2A(?)+B(?)?xC(g)△H<0,平衡时M中A、B、C的物质的量之比为1:3:4,下列判断不正确的是( )| A、x=4 |
| B、若N中气体的密度如图Ⅲ所示,则A、B只有一种是气态 |
| C、若A为气体,B为非气体,则平衡时M、N中C的物质的量相等 |
| D、若A、B均为气体,平衡时M中A的转化率大于N中A的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | C | |
| B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com