
下列离子方程式的书写正确的是
A.实验室用大理石和稀盐酸制取CO2:CO32-+2H+=CO2↑+H2O
B.向H2O中加入Na2O2固体:2Na2O2+2H2O=2Na++2OH-+2O2↑
C.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
D.SiO2与NaOH溶液反应:SiO2+2OH-=SiO32-+H2O
D
【解析】
试题分析:A.大理石难溶于水,不能写成离子形式,离子方程式应该为CaCO3+2H+=Ca2++CO2↑+H2O,错误;B.向H2O中加入Na2O2固体,应该形成4mol的NaOH,不符合质量守恒定律,离子方程式是:2Na2O2+2H2O=4Na++4OH-+2O2↑,错误;C.HClO是弱酸,应该下化学式,氯气与水反应的离子方程式是:Cl2+H2O=H++Cl-+HClO,错误. D.SiO2与NaOH溶液反应:SiO2+2OH-=SiO32-+H2O符合事实,拆写无误,正确。
考点:考查列离子方程式的书写的正误判断的知识。
考点分析: 考点1:离子方程式 试题属性

科目:高中化学 来源:2014-2015学年湖北省七市教科研协作体高三3月联考化学试卷(解析版) 题型:填空题
各种污染日趋严重,防止污染、改善水质的主要措施是对废气,废水进行处理.
Ⅰ.已知:汽车尾气处理的反应之一:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0
N2(g)+2CO2(g) △H<0
将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生上述反应,反应过程中部分物质的浓度变化如下左图所示.
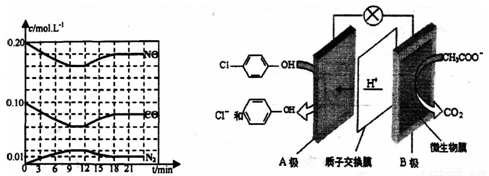
①该反应第一次达到平衡时的平衡常数为__________。
②第12min时改变的条件是___________(填“升温”、“降温”),判断的依据是____________________。
③在第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将_____移动(填“正向”、“逆向”或“不”).
Ⅱ.含有乙酸钠和对氯苯酚 的酸性废水,可利用微生物电池法除去,其原理如上右图所示
的酸性废水,可利用微生物电池法除去,其原理如上右图所示
①B是电池的______极(填“正”或“负”);
②酸性条件下,A极的电极反应式为______________________________。
③设电极两边溶液分别为1L,反应一段时间后,A极区溶液的pH从4变到1,此过程中处理的乙酸钠的质量为_________g 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
利用下列图示进行相应实验,能达到目的的是

A.用图1可萃取碘水中的碘
B.用图2可除去NO2中的NO
C.用图3制取并收集干燥纯净的NH3
D.用图4配制100mL一定物质的量浓度的稀硫酸
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,离子方程式如下(未配平):
MnO4-+ Fe2++ H+ = Mn2++ Fe3++ H2O
下列说法正确的是
A.MnO4-是氧化剂,Fe3+是还原产物
B.Mn2+的还原性强于Fe2+
C.离子方程式中按物质顺序的化学计量数是:1、5、8、1、5、4
D.生成1 mol 水时,转移2.5 mol电子
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.单质铝在空气中比较耐腐蚀,所以铝是不活泼金属
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.Na2CO3固体中含有的少量NaHCO3,可用加热法除去
D.钠在不同条件下与氧气的反应,产物只得到Na2O
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
下列物质转化关系中,需要加入氧化剂才能实现的是
A.Na2O2 →O2 B.MnO4-→Mn2+ C.Fe2+→Fe3+ D.CO2→HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:填空题
(14分)Q、R、X、Y、Z五种元素的原子序数依次递增。已知:① Z的原子序数为29,而Q、R、X、Y均为短周期主族元素;② R原子有3个未成对电子;③ Q、X原子p轨道的电子数分别为2和4;④ Y原子价电子(外围电子)排布为msnmpn。请回答下列问题:
(1)R的氢化物RH3中R采取______杂化,其键角_____109°28′(选填“>”、“=”或者“<”)。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是(选填字母代号)_____。
a.稳定性:甲>乙;沸点:甲>乙
b.稳定性:甲>乙;沸点:甲<乙
c.稳定性:甲<乙;沸点:甲<乙
d.稳定性:甲<乙;沸点:甲>乙
(3)下列与H2X分子互为等电子体的微粒有(选填字母代号) 。
a.CH4 b.H2S c.NO2 d.NH2-
(4)由X和Y形成的化合物属于________晶体(填晶体类型),30 g该晶体中有_____mol共价键。
(5)Z是 (填元素符号),它位于周期表的 区,其晶体的三维堆积模型见下图,

称之为面心立方最密堆积,其配位数为 。Z2+的外围电子排布式是____________。1个Z2+与4个RH3以配位键结合形成_________________离子(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
下列措施肯定能使化学反应速率增大的是
①增大反应物的量 ②增大压强 ③升高温度 ④使用正催化剂
A.①②③ B.③④ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三一模理综化学试卷(解析版) 题型:选择题
下列关于电化学的叙述正确的是

A.图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红
B.图②装置可以验证牺牲阳极的阴极保护法
C.图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH-
D.分别给上述4个装置的铁电极附近滴加少量K3[Fe(CN)6]溶液,②④出现蓝色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com