
【题目】某固体酸燃料电池以NaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表为:2H2 + O2 = 2H2O,下列有关说法正确的是

A. 电子通过外电路从b极流向a极
B. 每转移0.1mol电子,消耗1.12L的H2
C. b极上的电极反应式为: O2 + 2H2O + 4e- = 4OH-
D. H+由a极通过固体酸电解质传递到b
【答案】D
【解析】
根据电池总反应:2H2+O2=2H2O可知:通入氢气的一极为电池的负极,发生氧化反应,反应为H2-2e-=2H+,通入氧气的一极为电池的正极,发生还原反应,反应为O2+4e-+4H+=2H2O。
A.通入氢气的一极为负极,则a为正极,b为负极,电子的流向由负极经外电路流向正极,由b极经外电路流向a极,A项错误;
B.每转移0.1mol电子,消耗0.05mol的H2,标准状况下的体积为1.12L,但没有说明是否为标准状况,则气体的体积不一定为1.12L。B项错误;
C.中间为固体电解质,该电池为酸性电池,b极上的电极反应式为:O2+4e-+4H+=2H2O,C项错误;
D.a极氢气失电子生成H+,阳离子向正极移动,b为正极。所以H+由a极通过固体酸电解质传递到b极,D项正确;
本题答案选D。
电化学中阴阳离子的移动方向 | ||
离子种类 | 原电池 | 电解池 |
阳离子 | 向正极移动 | 向阴极移动 |
阴离子 | 向负极移动 | 向阳极移动 |


科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A.Ca2+、Cl-、K+、SO42-、CO32-B.H+、Mg2+、Na+、CO32-、SO42-
C.OH-、Cu2+、NO3、SO42-、CO32-D.Na+、H+、K+、SO42-、NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答:

已知:![]()
(1)上述过程中属于物理变化的是__________(填序号)。①分馏 ②裂解
(2)A的官能团是__________。
(3)反应II的化学方程式是________________________________________。
(4)D为高分子化合物,可以用来制造多种包装材料,其结构简式是__________。
(5)E是有香味的物质,在实验室可用下图装置制取。

①反应IV的化学方程式是________________________________________。
②在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D的单质颜色相同的淡黄色固态化合物。
试根据以上叙述回答:
(1)写出AB2的电子式:___________;
(2)用电子式表示C2B的形成过程:____________。
(3)写出C单质点燃时与B单质充分反应的化学方程式:___________。
(4)写出淡黄色固态化合物与水反应的化学方程式:___________。
(5)请设计简单实验,比较元素B、D的金属性(或非金属性)强弱:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的个数是( )
①MgSO4溶液 ②NaCl溶液 ③CuSO4溶液 ④饱和澄清石灰水
A.1B.2C.3D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数。X与Y位于不同周期,且X、Y、W原子最外层电子数之和恰好等于Z元素的核电荷数,X与W的最高化合价之和为8,元素Z的单质是目前使用量最大的主族金属元素单质。下列说法中正确的是
A. 离子化合物YX4W溶于水后,得到的溶液呈碱性
B. 化合物YW3为共价化合物,电子式为![]()
C. Y、Z形成的一种化合物强度高,热膨胀系数小,是良好的耐热冲击材料
D. 工业上常用电解Z与W形成的化合物的方法制取单质Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
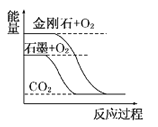

据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应 B. 白磷比红磷稳定
C. S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)=SO2(g) ΔH2 则ΔH1>ΔH2 D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 molA气体和2mol B气体在2L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)═2C(g)。若经2s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol·L-1
A. ①③B. ①④C. ②③D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com