
 2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.
2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.| 温度/ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
分析 (1)分析图表数据随温度升高二氧化硫转化率减小,平衡逆向进行,依据平衡原理分析判断反应热量变化;
(2)转化率=$\frac{消耗量}{起始量}$,平衡量=起始量-消耗量计算得到;
(3)①尾气中SO2与氨水恰好反应得到弱碱性的(NH4)2SO3溶液,依据溶液中物料守恒、电荷守恒、离子浓度大小比较依据分析判断选项;
②a.二氧化硫溶于水生成亚硫酸具有还原性,被二氧化锰氧化为硫酸,二氧化锰被还原为锰离子;
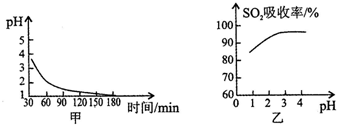
b.二氧化硫被氧化为硫酸溶液PH减小,依据图象分析PH增大有利于二氧化硫的吸收,酸性越强越有利于二氧化硫逸出.
解答 解:(1)图表数据随温度升高二氧化硫转化率减小,平衡逆向进行,逆反应为吸热反应,正反应为放热反应,
故答案为:放热;
(2)400℃,1.01×105Pa时,将含10mol SO2的原料气通入一密闭容器中进行反应,转化率=99.2%,平衡时SO2的物质的量=10mol-10mol×99.2%=0.08mol,
故答为:0.08;
(3)①用氨水吸收上述尾气,若尾气中SO2与氨水恰好反应得到弱碱性的(NH4)2SO3溶液,
a.溶液中氮元素和硫元素遵循物料守恒,氮元素物质的量和硫元素物质的量之比为2:1,c(NH4+)+c(NH3•H2O)=2[c(SO32-)+c(HSO3-)+c(H2SO3)],故a正确;
b.溶液中存在电荷守恒,c(NH4+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),故b错误;
c.弱碱性的(NH4)2SO3溶液中离子浓度大小为:c(NH4+)>c(SO32-)>c(OH-)>c(H+),故c正确;
故答案为:ac;
②a.二氧化硫溶于水生成亚硫酸具有还原性,被二氧化锰氧化为硫酸,二氧化锰被还原为锰离子,用MnO2与水的悬浊液吸收上述尾气并生产MnSO4,反应的化学方程式为:H2O+SO2=H2SO3 MnO2+H2SO3=MnSO4+H2O;
故答案为:H2O+SO2=H2SO3、MnO2+H2SO3=MnSO4+H2O;
b.图甲中pH变化是因为吸收中有部分SO2转化为H2SO4生成H2SO4反应的化学方程式为:2SO2+O2+2H2O=2H2SO4,二氧化硫被氧化为硫酸溶液PH减小,依据图象分析PH增大有利于二氧化硫的吸收,酸性越强越有利于二氧化硫逸出,由图乙可知pH的降低,酸性增强,抑制亚硫酸电离,促进亚硫酸分解,溶液中存在SO2+H2O?H2SO3?H++HSO3-,当溶液中酸性增强,平衡向左移动,使SO2气体从体系中逸出;
故答案为:2SO2+O2+2H2O=2H2SO4;不利于;溶液中存在SO2+H2O?H2SO3?H++HSO3-,当溶液中酸性增强,平衡向左移动,使SO2气体从体系中逸出.
点评 本题考查了化学平衡影响因素分析,平衡计算,电解质溶液中电荷守恒、物料守恒、离子浓度大小比较,氧化还原反应原理的分析应用,掌握基础是关键,题目难度中等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命.以甲醇为原料制取高纯H2是重要研究方向.
以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命.以甲醇为原料制取高纯H2是重要研究方向.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 甲 | 乙 | 丙 | 结论 | |
| A | 水 | 电石 | 溴水 | 稳定性:H2O>C2H2>Br2 |
| B | 盐酸 | 硫化亚铁 | 溴水 | 还原性:Cl->Br->S2- |
| C | 浓盐酸 | 高锰酸钾 | 溴化钾溶液 | 氧化性:高锰酸钾>Cl2>Br2 |
| D | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
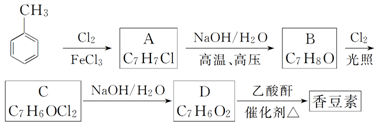
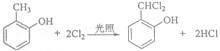 ;
;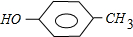 和
和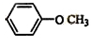 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com